右图是关于反应A2(g)+3B2(g)===2C(g)△H<0的平衡移动图形 影响平衡移动的原因是(
右图是关于反应A2(g)+3B2(g)===2C(g)△H<0的平衡移动图形,影响平衡移动的原因是( )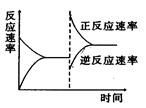
|
参考解答
| D |
试题分析:根据图像可知,改变条件后,正反应速率增大,逆反应速率减小,平衡向正反应方向移动,所以改变的条件是增大反应物浓度,同时减小生成物浓度,答案选D。 点评:该题是中等难度的试题,试题基础性强,主要是考查学生对可逆反应图像的熟悉了解程度,以及灵活运用基础知识解决实际问题的能力。该题的关键是明确图像的变化趋势,然后结合题意具体问题、具体分析即可,有利于培养学生的逻辑推理能力。 |
相似问题
某温度下 将2mol A和2.8 mol B充入体积为2 L的恒容密闭容器中 发生如下反应:aA(g
某温度下,将2mol A和2 8 mol B充入体积为2 L的恒容密闭容器中,发生如下反应:aA(g)+B(g)2C(g)+ D(s) ,5 min后达到平衡。平衡时A为1 6m
可逆反应A(?)+aB(g) C(g)+D(g) 其中a为正整数。反应过程中 当其他条件不变时 C的
可逆反应A(?)+aB(g) C(g)+D(g),其中a为正整数。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。试回答下列问题
将4mol A气体和2mol B气体在2L的密闭容器内混合 并在一定条件下发生如下反应:2A(g)+
将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)2C(g),若经2s后测得C的浓度为0 6mol·L-1,现有下列几种说法
氨气是重要化工产品之一。传统的工业合成氨技术的反应原理是:N2(g)+3H2(g)2NH3(g) Δ
氨气是重要化工产品之一。传统的工业合成氨技术的反应原理是:N2(g)+3H2(g)2NH3(g) ΔH=-92 4 kJ mol。在500 ℃、20 MPa时,将N2、H2置于一
如图是可逆反应X2+3Y22Z2在反应过程中的反应速率V与时间(t)的关系曲线 下列叙述正确的是A.
如图是可逆反应X2+3Y22Z2在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是A.t1时,只有正方向反应B.t2时,反应到达限度C.t2-t3,反












