设反应①Fe(s)+CO2(g)FeO(s)+CO(g)的平衡常数为K1 反应②Fe(s)+H2O(
设反应①Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+CO(g)的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数为K2。在不同温度下,K1、K2的值如下 FeO(s)+H2(g)的平衡常数为K2。在不同温度下,K1、K2的值如下 |
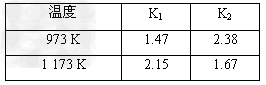 |
| (1)从上表可以推断:反应①是________(填“吸”、“放”)热反应。 (2)现有反应③CO2(g)+H2(g) 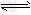 CO(g)+H2O(g),写出该反应的平衡常数K3的数学表达式:K3=________。 CO(g)+H2O(g),写出该反应的平衡常数K3的数学表达式:K3=________。(3)根据反应①与②,可推导出K1、K2与K3之间的关系式。据此关系式及上表数据,也能推断出反应③是“吸热”还是“放热”反应。问:要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有________(填写序号)。 A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度 D.升高温度 E.使用合适的催化剂 F.设法减少CO的量 (4)图1、2表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况: |
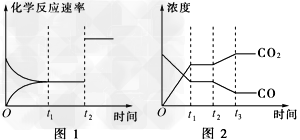 |
| ①图1中t2时刻发生改变的条件是 ___________________________________。 ②图2中t2时刻发生改变的条件是 _____________________。 |
参考解答
| (1)吸 (2)“略” (3)DF (4)①加入催化剂或增大体系的压强;②降低温度或增加水蒸气的量或减少氢气的量 |
相似问题
一氧化氮与一氧化碳都是汽车尾气里的有害物质 它们能缓慢地起反应生成氮气和二氧化碳。对此反应 下列叙述
一氧化氮与一氧化碳都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳。对此反应,下列叙述中正确的是[ ]A.使用催化剂能改变平衡常数
(1)二氧化硫的催化氧化的过程如图1所示 其中a c二步的化学方程式可表示为:SO2+V2O5?SO
(1)二氧化硫的催化氧化的过程如图1所示,其中a、c二步的化学方程式可表示为:SO2+V2O5?SO3+V2O44VOSO4+O2?2V2O5+4SO3.该反应的催化剂是______(写化学
如图是反应 A2+B2═2AB 在不同温度和压强下 AB体积分数(AB%)的变化情况.其中a b 曲
如图是反应A2+B2═2AB在不同温度和压强下,AB体积分数(AB%)的变化情况.其中a、b曲线为相同压强、不同温度时的变化情况,c曲线是保持与b相同温度时从时
单质碘与红磷在常温下混合不反应 但滴入几滴水后能剧烈反应 生成HI和H3PO3。但实验室制取氢碘酸的
单质碘与红磷在常温下混合不反应,但滴入几滴水后能剧烈反应,生成HI和H3PO3。但实验室制取氢碘酸的方法是把H2S通入I2水中,过滤生成的硫,可得质量分数
300℃时 将2mol A和2mol B两种气体混合于2 L密闭容器中 发生如下反应:3A(g)+B
300℃时,将2mol A和2mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g) △H=Q,2 min末达到平衡,生成0.8 mol D。(1)












