(1)二氧化硫的催化氧化的过程如图1所示 其中a c二步的化学方程式可表示为:SO2+V2O5?SO
(1)二氧化硫的催化氧化的过程如图1所示,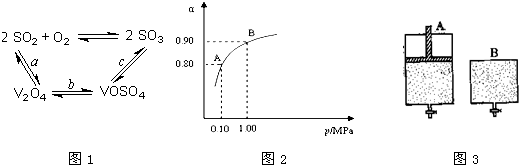 其中a、c二步的化学方程式可表示为:SO2+V2O5?SO3+V2O4 4VOSO4+O2?2V2O5+4SO3. 该反应的催化剂是______(写化学式) (2)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图2所示.将2.0molSO2和1.0molO2置于5L密闭容器中,反应达平衡后,体系总压强为0.10MPa.试计算反应2SO3?2SO2+O2在550℃时的平衡常数K=______. (3)550℃时,将2.0molSO2和1.0molO2置于5L密闭容器中,反应达平衡后,下列措施中能使
A.升高温度B.充入He(g),使体系总压强增大 C.再充入2molSO2和1molO2D.再充入1molSO2和1molO2 (4)维持温度不变条件下使之发生如下反应:2SO2+O2?2SO3,有两只密闭容器A和B.A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等(如图3所示). 试填写下列空格: A容器达到平衡时所需的时间比B容器______(填:“短”或“长”);平衡时A容器中SO2的转化率比B容器______(填:“大”或“小”);达到所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数______(填“增大”、“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数______. |
参考解答
| (1)依据图1中的转化关系和化学方程式分析,V2O5参与反应先做氧化剂把二氧化硫氧化为三氧化硫,本身被还原为图中产物V2O4;根据氧化还原反应的实质写出并配平a步化学方程式SO2+V2O5?SO3+V2O4;C是VOSO4转化为SO3,此过程需要重新生成催化剂V2O5,故答案为:V2O5; (2)体系总压强为0.10M Pa,此时二氧化硫的转化率为80% 2SO2+O2
起始量(mol) 2 1 0 变化量 (mol)2×0.8 0.8 2×0.8 平衡量 (mol) 0.4 0.2 1.6 平衡时各物质的浓度为:[SO2=0.08mol/L,[O2=0.04mol/L,[SO3=0.32mol/L 代入平衡常数的计算式得到 平衡常数K=
则反应2SO3?2SO2+O2在550℃时的平衡常数K=
故答案为:2.5×10-3; (3)2SO2+O2
A.升高温度,平衡逆向进行,
B.充入He(g),使体系总压强增大,分压不变,平衡不动,
C.再充入2molSO2和1molO2,相当于增大压强平衡正向进行,
D.再充入1molSO2和1molO2,二氧化硫转化率增大,
故答案为:故CD; (4)因A容器保持恒压,反应过程中体积变小,浓度增大,根据浓度越大,化学反应速率越快,到达平衡的时间越短,所以达到平衡所需时间A比B短,若A容器保持恒容,两容器建立的平衡等效,而实际上A容器体积减少,压强增大,平衡向正反应方向移动,所以A中SO2的转化率比B大;平衡后,向两容器中通入等量的原反应气体,达到平衡后,A中建立的平衡与原平衡等效,所以SO3的体积分数不变,B容器中建立的平衡相当于在原平衡的基础上增大压强,平衡正向移动,B容器中SO3的体积分数增大; 故答案为:短;大;不变;增大. |
相似问题
如图是反应 A2+B2═2AB 在不同温度和压强下 AB体积分数(AB%)的变化情况.其中a b 曲
如图是反应A2+B2═2AB在不同温度和压强下,AB体积分数(AB%)的变化情况.其中a、b曲线为相同压强、不同温度时的变化情况,c曲线是保持与b相同温度时从时
单质碘与红磷在常温下混合不反应 但滴入几滴水后能剧烈反应 生成HI和H3PO3。但实验室制取氢碘酸的
单质碘与红磷在常温下混合不反应,但滴入几滴水后能剧烈反应,生成HI和H3PO3。但实验室制取氢碘酸的方法是把H2S通入I2水中,过滤生成的硫,可得质量分数
300℃时 将2mol A和2mol B两种气体混合于2 L密闭容器中 发生如下反应:3A(g)+B
300℃时,将2mol A和2mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g) △H=Q,2 min末达到平衡,生成0.8 mol D。(1)
“低碳循环”引起各国的高度重视 而如何降低大气中CO2的含量及有效地开发利用CO2 引起了全世界的普
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课
在体积 温度都相同的条件下有下列反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径
在体积、温度都相同的条件下有下列反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始












