单质碘与红磷在常温下混合不反应 但滴入几滴水后能剧烈反应 生成HI和H3PO3。但实验室制取氢碘酸的
| 单质碘与红磷在常温下混合不反应,但滴入几滴水后能剧烈反应,生成HI和H3PO3。但实验室制取氢碘酸的方法是把H2S通入I2水中,过滤生成的硫,可得质量分数为50%的氢碘酸 (1)写出实验室制取氢碘酸的化学方程式______________________; (2)氢碘酸在空气中放置易易氧化变质,写出可能发生反应的化学方程式___________________________; (3)为防止氢碘酸在空气中氧化变质,可在氢碘酸中加入少量___________,写出有关反应的化学方程式__________________________。 (4)在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表: |
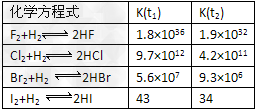 |
| ①已知t2>t1,HX的生成反应是__________ 反应(填“吸热”或“放热”)。 ②共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是_______________。 ③仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_________________(选填字母)。 a.在相同条件下,平衡时X2的转化率逐渐降低 b.X2与H2反应的剧烈程度逐渐减弱 c.HX的还原性逐渐减弱 d.HX的稳定性逐渐减弱 |
参考解答
| (1)I2+H2S==2HI+S↓ (2)4HI+O2==I2+2H2O (3)红磷;3I2+2P+3H2O==6HI+2H3PO3 (4)①放热;②HF、HCl、HBr、HI;③ad |
相似问题
300℃时 将2mol A和2mol B两种气体混合于2 L密闭容器中 发生如下反应:3A(g)+B
300℃时,将2mol A和2mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g) △H=Q,2 min末达到平衡,生成0.8 mol D。(1)
“低碳循环”引起各国的高度重视 而如何降低大气中CO2的含量及有效地开发利用CO2 引起了全世界的普
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课
在体积 温度都相同的条件下有下列反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径
在体积、温度都相同的条件下有下列反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始
下列关于化学平衡常数的说法中错误的是( )A.化学平衡常数K只与温度有关 随温度的升高 K可能增大
下列关于化学平衡常数的说法中错误的是( )A.化学平衡常数K只与温度有关,随温度的升高,K可能增大、减小或不变B.催化剂不能改变平衡常数的大小C.
氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示(1)甲烷和水蒸气反应生成二氧化碳和
氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是______________。(2)第Ⅱ步












