已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:温度/ ℃700800830
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下: C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题: (1)该反应的平衡常数表达式K= , △H 0(填“<”“ >”“ =”); (2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时 c(A)= mol·L-1, C的物质的量= mol; 若经一段时间后,反应达到平衡,则此时A的转化率= ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率 ( 填“变大”或“变小”或“不变”); (3)判断该反应达到平衡的依据为 (填正确选项前的字母): A.压强不随时间改变 B.气体的密度不随时间改变 C.c(A)不随时间改变 D.单位时间里生成C和D的物质的量相等 (4)1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为 。 A(g)+B(g)的平衡常数的值为 。 |
参考解答
(1)K= 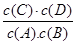 < < (2)0.022 0.09 80% 不变 (3)C (4)2 .5 |
试题分析:(1)可逆反应达到平衡状态时各生成物浓度的幂指数的乘积与各反应物浓度幂指数的乘积的比。该反应的化学平衡常数K= 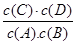 。因为升高温度,化学平衡常数减小,说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应。所以该反应的正反应为放热反应。所以△H<0.(2)v(A)=0.003 mol·L-1·s-1,△c(A)= v(A)×△t=0.003 mol·L-1·s-1×6s=0.018mol/L则6s时c(A)=(0.20mol÷5 L)-0.018mol/L=0.022mol/L.C的物质的量0.018mol/L×5 L= 0.09mol。因为在830℃时化学平衡常数K=1.0.假设在反应的过程中A消耗的物质的量为x 则达到平衡时各物质的物质的量分别是A:(0.20-x)mol;B:(0.80-x)mol;C:xmol;D:xmol.由于各物质的方程式前边的系数都为1,所以达到平衡时的物质的量的比等于浓度的比。X2÷[(0.20-x)×(0.80-x)=1.0.解得x=0.16.所以A的转化率为(0.16÷0.20)×100%=80%。如果这时向该密闭容器中再充入1 mol氩气,因为容器的容积不变。A的浓度不变,所以平衡不发生移动。故平衡时A的转化率也不变。(3)A.因为该反应是个反应前后气体体积相等的可逆反应,所以无论反应是否达到平衡,容器内气体的压强都不会发生改变。错误。B.由于在反应前后气体的体积不变,反应遵循质量守恒定律,质量也不变,因此任何时刻,无论反应是否达到平衡,气体的密度都不改变。错误。C.若反应未达到平衡,则 c(A)就会发生改变。现在c(A)不随时间改变,说明反应达到了平衡状态。正确。D.在方程式中,C和D都是生成物,系数相同,所以在任何时间段内单位时间里生成C和D的物质的量总是相等,因此不能以此为标准判断反应是否达到平衡状态。错误。故正确的选项为C。(4)在1200℃时A(g)+B(g) 。因为升高温度,化学平衡常数减小,说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应。所以该反应的正反应为放热反应。所以△H<0.(2)v(A)=0.003 mol·L-1·s-1,△c(A)= v(A)×△t=0.003 mol·L-1·s-1×6s=0.018mol/L则6s时c(A)=(0.20mol÷5 L)-0.018mol/L=0.022mol/L.C的物质的量0.018mol/L×5 L= 0.09mol。因为在830℃时化学平衡常数K=1.0.假设在反应的过程中A消耗的物质的量为x 则达到平衡时各物质的物质的量分别是A:(0.20-x)mol;B:(0.80-x)mol;C:xmol;D:xmol.由于各物质的方程式前边的系数都为1,所以达到平衡时的物质的量的比等于浓度的比。X2÷[(0.20-x)×(0.80-x)=1.0.解得x=0.16.所以A的转化率为(0.16÷0.20)×100%=80%。如果这时向该密闭容器中再充入1 mol氩气,因为容器的容积不变。A的浓度不变,所以平衡不发生移动。故平衡时A的转化率也不变。(3)A.因为该反应是个反应前后气体体积相等的可逆反应,所以无论反应是否达到平衡,容器内气体的压强都不会发生改变。错误。B.由于在反应前后气体的体积不变,反应遵循质量守恒定律,质量也不变,因此任何时刻,无论反应是否达到平衡,气体的密度都不改变。错误。C.若反应未达到平衡,则 c(A)就会发生改变。现在c(A)不随时间改变,说明反应达到了平衡状态。正确。D.在方程式中,C和D都是生成物,系数相同,所以在任何时间段内单位时间里生成C和D的物质的量总是相等,因此不能以此为标准判断反应是否达到平衡状态。错误。故正确的选项为C。(4)在1200℃时A(g)+B(g) C(g)+D(g)的平衡常数 C(g)+D(g)的平衡常数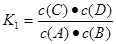 反应C(g)+D(g) 反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为 A(g)+B(g)的平衡常数的值为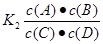 ;可见K1、K2互为倒数。因为此时K1=0.4,所以K2=1÷0.4=2 .5。 ;可见K1、K2互为倒数。因为此时K1=0.4,所以K2=1÷0.4=2 .5。 |
相似问题
一定条件下 在体积为5 L的密闭容器中 气态物质A B C的物质的量n(mol)随时间t的变化如图1
一定条件下,在体积为5 L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如图1所示。已知达平衡后,降低温度,A的体积百分含量将减小。(1)
已知合成氨反应N2(g)+3H2(g)2NH3(g) ΔH='-92.20' kJ·mol-1 在某
已知合成氨反应N2(g)+3H2(g)2NH3(g) ΔH="-92 20" kJ·mol-1,在某温度下2 L的密闭容器中进行,测得如下数据:时间(h)物质的量(mol) 01234N21 50n11 20n
某化学反应 3 A 2 B + D在四种不同条件下进行 B D的起始浓度为0。反应物A 的浓度
某化学反应 3 A 2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:根据上述数据,完成下列
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中 该铝片与
把在空气中久置的铝片5 0 g投入盛有500 mL 0 5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回
一定温度下有可逆反应:A(g)+2B(g) 2C(g)+D(g) 。现将5molA和10molB加入
一定温度下有可逆反应:A(g)+2B(g) 2C(g)+D(g) 。现将5molA和10molB加入一体积为2L的密闭容器中,反应至10min时改变某一条件,C的物质的量浓度随时间












