一定条件下 在体积为5 L的密闭容器中 气态物质A B C的物质的量n(mol)随时间t的变化如图1
一定条件下,在体积为5 L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如图1所示。已知达平衡后,降低温度,A的体积百分含量将减小。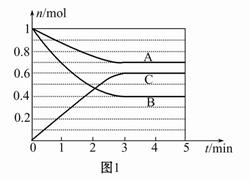 (1)根据上图数据,写出反应的化学方程式 ; 从反应开始到平衡时的平均速率v(C)= 。 (2)该反应的ΔH 0(填“>”、“<”或“=”)。 (3)此反应平衡常数的表达式为K= 。 (4)该反应的反应速率v和时间t的关系如图2所示: 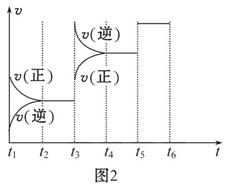 ①根据上图判断,在t3时刻改变的外界条件是 。 ②A的转化率最大的一段时间是 。 ③各阶段的平衡常数如表所示:  K1、K2、K3之间的关系为: (用“>”、“<”或“=”连接)。 |
参考解答
(1)A+2B 2C 0.04 mol·L-1·min-1 2C 0.04 mol·L-1·min-1(2)< (3) 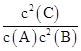 (4)①升高温度 ②t2~t3 ③K1>K2=K3 (4)①升高温度 ②t2~t3 ③K1>K2=K3 |
(1)根据图像可知,A、B为反应物,C为生成物,从反应开始到达平衡的过程中A、B、C的物质的量的变化为0.3 mol、0.6 mol、0.6 mol,所以反应方程式为A+2B 2C。C的平均速率为0.6 mol/(5 L×3 min)='0.04' mol·L-1· 2C。C的平均速率为0.6 mol/(5 L×3 min)='0.04' mol·L-1·min-1。 (2)反应达到平衡后,降低温度,A的体积分数减小,说明降低温度平衡向正反应方向移动,正反应为放热反应。 (3)该反应的平衡常数表达式为K= 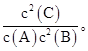 (4)①t3时刻改变条件,正逆反应速率都增大,且平衡向逆反应方向进行,则改变的条件是升高温度。 ②t5时刻改变的条件是使用催化剂,A的转化率不变,故整个过程中A的转化率最大的一段时间是t2~t3。 因为t3升高温度,t5使用催化剂,该反应为放热反应所以K1>K2=K3 |
相似问题
已知合成氨反应N2(g)+3H2(g)2NH3(g) ΔH='-92.20' kJ·mol-1 在某
已知合成氨反应N2(g)+3H2(g)2NH3(g) ΔH="-92 20" kJ·mol-1,在某温度下2 L的密闭容器中进行,测得如下数据:时间(h)物质的量(mol) 01234N21 50n11 20n
某化学反应 3 A 2 B + D在四种不同条件下进行 B D的起始浓度为0。反应物A 的浓度
某化学反应 3 A 2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:根据上述数据,完成下列
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中 该铝片与
把在空气中久置的铝片5 0 g投入盛有500 mL 0 5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回
一定温度下有可逆反应:A(g)+2B(g) 2C(g)+D(g) 。现将5molA和10molB加入
一定温度下有可逆反应:A(g)+2B(g) 2C(g)+D(g) 。现将5molA和10molB加入一体积为2L的密闭容器中,反应至10min时改变某一条件,C的物质的量浓度随时间
在25℃时 向100mL含氯化氢14.6g的盐酸里 放入5.6g铁粉(不考虑反应前后溶液体积的变化)
在25℃时,向100mL含氯化氢14 6g的盐酸里,放入5 6g铁粉(不考虑反应前后溶液体积的变化),反应开始到2min末收集到H2 1 12L(标准状况),在此后,又经












