(16分)硫酸铜受热分解生成氧化铜和气体 受热温度不同 该气体成分也不同。气体成分可能含SO2 SO
(16分)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式,实验用到的仪器如下图所示:
【提出猜想】 I.所得气体的成分可能只含_________一种; II.所得气体的成分可能含有__________二种; III.所得气体的成分可能含有SO2、SO3、O2三种。 【实验探究】 实验操作过程(略)。已知实验结束时,硫酸铜完全分解。 请回答下列问题: (1)请你组装探究实验的装置,按从左至右的方向,行仪器接口连接顺序为__________(填序号); (2)若实验结束,B中量筒没有收集到水,则证明猜想__________正确; (3)实验过程,仪器C的作用是 ________________________; (4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:  请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式: ① 组_________________________________________________________________; ② 组_______________________________________________________________。 |
参考解答
| I。SO2;Ⅱ。SO2、O2。(1)①③④⑥⑤② (2)I (3)吸收SO2和三氧化硫气体 (4)①4CuSO4 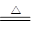 4CuO+2SO2↑+2SO3↑+O2↑ ②2CuSO4 4CuO+2SO2↑+2SO3↑+O2↑ ②2CuSO4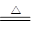 2CuO+2SO2↑+O2↑ 2CuO+2SO2↑+O2↑ |
| I.根据猜想Ⅲ可知,猜想I是所得气体的成分可能只含SO2一种,猜想Ⅱ是所得气体的成分可能含有SO2、O2两种。 (1)根据所给的装置可判断,碱石灰是吸收SO2或三氧化硫的,最后通过排水法收集气体氧气,以测量氧气的体积,所以正确的顺序是①③④⑥⑤②。 (2)B中量筒没有收集到水,说明没有氧气生成,所以猜想I是正确的。 (3)仪器C含有碱石灰,用来吸收SO2和三氧化硫气体。 (4)①中氧气是0.01mol,转移电子是0.04mol,所以一定生成0.02molSO2。其质量是1.28g,所以三氧化硫的质量是2.88g-1.28g=1.6g,物质的量是0.02mol,所以方程式为4CuSO4 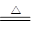 4CuO+2SO2↑+2SO3↑+O2↑。 4CuO+2SO2↑+2SO3↑+O2↑。②中氧气是0.02mol,转移电子是0.08mol,所以一定生成0.04molSO2。其质量是2.56g,所以没有三氧化硫生成,则方程式为2CuSO4 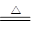 2CuO+2SO2↑+O2↑ 2CuO+2SO2↑+O2↑ |
相似问题
(10分)已知某白色混合物粉末中含有CuSO4 K2SO4 NH4HCO3 NH4Cl NaCl五种
(10分)已知某白色混合物粉末中含有CuSO4、K2SO4、NH4HCO3、NH4Cl、NaCl五种物质中的两种,且物质的量之比为1:1。请完成下述探究混合物组成的实验。仅限
(17分)实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物 极易与空气中水蒸汽和CO2反应
(17分)实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸汽和CO2反应而变质。某同学对一瓶久置的“碱石灰”作了如下探究:(1)
(14分)用一定物质的量浓度的NaOH溶液滴定10.00 mL已知浓度的盐酸 滴定结果如图所示。回答
(14分)用一定物质的量浓度的NaOH溶液滴定10 00 mL已知浓度的盐酸,滴定结果如图所示。回答下列问题:(1)有关滴定的操作可分解为如下几步,并补充完
(1) 实验过程中 可能观察到的主要现象有:①
(1) 实验过程中,可能观察到的主要现象有:①;②;③;④;(2) 用该装置做铜与浓硝酸反应的实验,最突出的优点是。(3) 若要验证最终得到的气体生成物
(10分)现有X Y Z三种非金属元素 A B C三种金属元素 已知有如下情况:(1)X Y Z的单
(10分)现有X、Y、Z三种非金属元素,A、B、C三种金属元素,已知有如下情况:(1)X、Y、Z的单质在常温下均为气体(2)X的单质在Z的单质中燃烧,生成XZ,燃烧时













