一个课外兴趣小组对某只含Cu Fe的合金成分含量进行分析(装置见图)。方法:按图示取a g的Cu F
一个课外兴趣小组对某只含Cu、Fe的合金成分含量进行分析(装置见图)。 方法:按图示取a g的Cu、Fe合金和纯铜做为电极,电解液里是含足量的Cu2+离子。接通电源进行实验,一直通电到Cu、Fe合金刚好全部溶解时为止。实验结果是:发现在通电实验过程中两电极均无气体产生,纯铜电极上质量增加19.2g,电解液的质量减少0.8g。请回答: (1)写出电极反应:阳极 ; 阴极 。 (1)该合金中Cu和Fe的物质的量之比是_________________________。 (3)若另取该合金a g把该Cu、Fe合金与足量的稀硝酸反应后,在溶液中再加入NaOH,能得到的最大沉淀量是________ _g。 |
参考解答
| (10分) (1)Fe-2e-=Fe2+、Cu-2e-=Cu2+;Cu2++2e-=Cu(2)2:1。 (3)30.3。 |
试题分析:(1)根据装置图可知,Cu、Fe合金和电源的正极相连,做阳极,失去电子,电极反应式是Fe-2e-=Fe2+、Cu-2e-=Cu2+;纯铜和电源的负极相连,做阴极,溶液中的铜离子得到电子,电极反应式是Cu2++2e-=Cu。 (2)设合金中Cu和Fe的物质的量分别是x和y,则19.2-64x-56y=0.8、2x+2y= 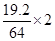 ,解得x=0.2.y=0.1,则合金中Cu和Fe的物质的量之比是2:1。 ,解得x=0.2.y=0.1,则合金中Cu和Fe的物质的量之比是2:1。(3)根据(2)可知,最终生成的测定是0.2mol氢氧化铜和0.1mol氢氧化铁,则质量是0.2mol×98g/mol+0.1mol×107g/mol=30.3g。 点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,旨在培养学生灵活运用电解原理解决实际问题的能力。该题的关键是明确电解的工作原理,然后结合题意灵活运用即可。该题的难点是计算。 |
相似问题
溶液中含有两种溶液质—氯化钠和硫酸 他们的物质的量之比为3:1。用石墨做电极电解该溶液时 根据反应产
溶液中含有两种溶液质—氯化钠和硫酸,他们的物质的量之比为3:1。用石墨做电极电解该溶液时,根据反应产物可明显分为三个阶段,则下列叙述不正确的是 A
高锰酸钾是锰的重要化合物和常用氧化剂 在实验室和医疗上有非常广泛的应用。以下是工业上用软锰矿(主要含
高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用。以下是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程:(1)
某同学为完成 2HCl+2Ag=2AgCl↓+H2↑反应 设计了下列四个实验如图所示你认为可行 的是
某同学为完成 2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验如图所示你认为可行 的是
(10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值 其实验方案的要点为:①
(10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值,其实验方案的要点为:①用直流电电解氯化铜溶液,所用仪器如图:②在电
下列描述中不符合生产实际的是A.电解水制氢气时 用铜作阳极 B.电解法精炼粗铜 用纯铜作阴极C
下列描述中不符合生产实际的是A.电解水制氢气时,用铜作阳极 B.电解法精炼粗铜,用纯铜作阴极C.电解饱和食盐水制烧碱,阴极上产生氢气D.在镀












