(10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值 其实验方案的要点为:①
| (10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值,其实验方案的要点为: ①用直流电电解氯化铜溶液,所用仪器如图: 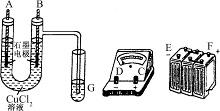 ②在电流为I A,通电时间为t s后,精确测得某电极上析出的铜的质量为m g. 试回答: (1)连接这些仪器的正确顺序为:(用图中标注仪器接线柱的英文字母表示,下同)E接________,C接________,________接F. (2)写出B电极上发生反应的离子方程式________________.G试管中淀粉KI溶液变化的现象为__________________,相应的离子方程式是__________________. (3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序是________.(选填下列操作步骤的编号) ①称量电解前电极质量 ②刮下电解后电极上的铜并清洗 ③用蒸馏水清洗电解后电极 ④低温烘干电极后称量 ⑤低温烘干刮下的铜后称量 ⑥再次低温烘干后称量至恒重 (4)已知电子的电荷量为1.6×10-19C.试列出阿伏伽德罗常数的计算表达式:NA=________. |
参考解答
| (1)D A B (2)2Cl--2e-===Cl2↑ 溶液变蓝 Cl2+2I-===2Cl-+I2 (3)①③④⑥ (4) 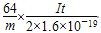 mol-1 mol-1 |
| (1)B电极上应产生Cl2:2Cl--2e-===Cl2↑,B极上流出电子,电子进入直流电源的正极,即F极,由此可得仪器连接顺序及电流方向。 (2)B中产生Cl2,Cl2进入G中与KI反应,有I2生成,I2使淀粉变蓝色。 (3)镀在A电极上的Cu是没必要刮下的,也无法刮干净,故②⑤两步须排除在外。 (4)因为析出Cu的物质的量=m/64mol,电子转移物质的量为m/64×2 mol,即m/64×2×NA个电子,由于电子的电荷量为1.6×10-19C,所以m/64×2×NA×1.6×10-19=It, 则NA= 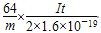 mol-1。 mol-1。 |
相似问题
下列描述中不符合生产实际的是A.电解水制氢气时 用铜作阳极 B.电解法精炼粗铜 用纯铜作阴极C
下列描述中不符合生产实际的是A.电解水制氢气时,用铜作阳极 B.电解法精炼粗铜,用纯铜作阴极C.电解饱和食盐水制烧碱,阴极上产生氢气D.在镀
Cu2O是一种半导体材料 某同学设计了制取Cu2O的电解装置示意图 总反应为2Cu+H2O==Cu2
Cu2O是一种半导体材料,某同学设计了制取Cu2O的电解装置示意图,总反应为2Cu+H2O==Cu2O+H2,下列说法正确的是A.铜电极连接直流电源的负极B.铜电极发生
电解CuCl2溶液时 如果阴极上有1.6g铜析出时 则阳极上产生气体的体积是( )A.0.2
电解CuCl2溶液时,如果阴极上有1 6g铜析出时,则阳极上产生气体的体积是( )A.0 28LB.0 56LC.0 14LD.11 2L
常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液 理论上两极所得气体的体积随时间变化的关
常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),
在下图装置中 若通电一段时间后乙装置左侧电极质量增加 则下列说法错误的是( )A.乙中左侧电极
在下图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是( )A.乙中左侧电极反应式:Cu2++2e-=CuB.电解过程中装置丙的pH无变化C.












