(10分)汽车尾气中含有CO和氮氧化物。治理尾气的方法是在排气管上安一个催化转化器 可发生如下反应:
| (10分) 汽车尾气中含有CO和氮氧化物。治理尾气的方法是在排气管上安一个催化转化器,可发生如下反应:2NO+2CO  N2+2CO2。 N2+2CO2。(1)2NO(g)+2CO(g)  N2(g)+2CO2(g)反应的平衡常数的表达式为: N2(g)+2CO2(g)反应的平衡常数的表达式为:K= 。 (2)已知:CO(g)+ 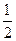 O2(g)=2CO2(g) △H=一283 kJ/mol O2(g)=2CO2(g) △H=一283 kJ/molN2(g)+O2(g)="2" NO(g) △H="+180" kJ/mol 则反应2NO(g)+2CO(g)  N2(g)+2CO2(g)△H= kJ/mol。 N2(g)+2CO2(g)△H= kJ/mol。(3)对于可逆反应2NO(g)+2CO(g)  N2(g)+2CO2(g),结合(2)中信息,下列说法正确的是 。 N2(g)+2CO2(g),结合(2)中信息,下列说法正确的是 。①升高温度,平衡常数增大 ②升高温度,逆反应速率降低 ③在单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 ④反应达到平衡后,其他条件不变,缩小容器容积,平衡向生成N2和CO2的方向移动 (4)下列说法正确的是 ①NO、CO、CO2均为酸性氧化物 ②CO2的大量排放会导致温室效应,所以应尽量选用公共交通,提倡低碳  出行 出行③汽车尾气中的氮氧化物主要是空气中的氮气与氧气在高温条件下生成的 (5)实验室可利用NaOH溶液吸收CO2,标准状况下2.24LCO2气体被1.5 L 0.1 mol/L NaOH溶液全部吸收(不考虑CO2溶于水),生成NaCO3的物质的量为 mol。 |
参考解答
(1) 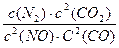 (2分) (2分)(2)-746(2分) (3)③④(2分) (4)②③(2分) (5)0.05(2分) |
| 略 |
相似问题
按图示装置 开关闭合后 导线中有电流通过且乙电极的电极反应式为:Fe-2e-=Fe2+的是( )甲
按图示装置,开关闭合后,导线中有电流通过且乙电极的电极反应式为:Fe-2e-=Fe2+的是( )甲乙丙(溶液)ACuFeFe2(SO4)3BFeFeCuCl2CZnFeH2SO4DCFeNaOHA.AB.BC.CD.D
将0.23 mol SO2和0.11 mol O2放入容积为1 L的密闭容器中 发生反应2SO2+O
将0 23 mol SO2和0 11 mol O2放入容积为1 L的密闭容器中,发生反应2SO2+O22SO3,在一定温度下,反应达到平衡,得到0 12 mol SO3,则反应的平衡常
下列装置中 溶液均为稀硫酸 可以构成原电池的是( )A.B.C.D.
下列装置中,溶液均为稀硫酸,可以构成原电池的是( )A.B.C.D.
(12分)自然界里氮的固定途径之一是在闪电的作用下 N2与O2反应生成NO。(1)在不同温度下 反应
(12分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。(1)在不同温度下,反应N2(g)+O2(g)2NO(g)△H=a kJ·mol-1的平衡常数K如下表
两个串联的电解池A和B 分别盛有AgNO3溶液和NaCl溶液 用惰性电极进行电解 当B池的阴极上收集
两个串联的电解池A和B,分别盛有AgNO3溶液和NaCl溶液,用惰性电极进行电解,当B池的阴极上收集到2.24 L(标准状况)气体时,在A池的阳极上析出物质多少克












