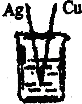
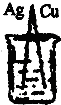下列装置中 溶液均为稀硫酸 可以构成原电池的是( )A.B.C.D.
下列装置中,溶液均为稀硫酸,可以构成原电池的是( )
|
参考解答
| 原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应. A.锌和铜在稀硫酸溶液中形成原电池反应,锌做负极,铜做正极,该装置能自发的进行氧化还原反应,所以能构成原电池,故A正确; B.铜和银与稀硫酸不反应,不能自发的进行氧化还原反应,该装置不符合原电池构成条件,所以不能构成原电池,故B错误; C.铜和银与稀硫酸不反应,不能自发的进行氧化还原反应,该装置不符合原电池构成条件,所以不能构成原电池,故C错误; D.该装置不能构成闭合回路,所以不能构成原电池,故D错误; 故选:A. |
相似问题
(12分)自然界里氮的固定途径之一是在闪电的作用下 N2与O2反应生成NO。(1)在不同温度下 反应
(12分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。(1)在不同温度下,反应N2(g)+O2(g)2NO(g)△H=a kJ·mol-1的平衡常数K如下表
两个串联的电解池A和B 分别盛有AgNO3溶液和NaCl溶液 用惰性电极进行电解 当B池的阴极上收集
两个串联的电解池A和B,分别盛有AgNO3溶液和NaCl溶液,用惰性电极进行电解,当B池的阴极上收集到2.24 L(标准状况)气体时,在A池的阳极上析出物质多少克
已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O 设计如图装置 进行下述操作:①
已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:①向(Ⅱ)烧杯中逐滴加入浓盐酸,发现微安表(G)指针偏转;②若改往(Ⅱ)烧
根据图回答 下列说法不正确的是( )A.此装置用于铁表面镀铜时 a为铁B.此装置用于电镀铜时 硫酸
根据图回答,下列说法不正确的是( )A.此装置用于铁表面镀铜时,a为铁B.此装置用于电镀铜时,硫酸铜溶液的浓度不变C.燃料电池中正极反应为12O2+2H
下列叙述中正确的是( )①锌跟稀硫酸反应的制取氢气 加入少量硫酸铜溶液能加快反应速率;②镀层破损后
下列叙述中正确的是( )①锌跟稀硫酸反应的制取氢气,加入少量硫酸铜溶液能加快反应速率;②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)铁更