参考解答
| B |
| 溶液的导电性强弱与溶液中阴阳离子的浓度大小和离子所带的电荷数有关系,溶液中氢离子最大的是硫酸中氢离子的浓度,所以选项B正确。 |
相似问题
化合物HIn在水溶液中因存在以下电离平衡 故可用作酸碱指示剂HIn(溶液) H+(溶液)+In-(溶
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂HIn(溶液) H+(溶液)+In-(溶液)红色黄色浓度为0 02 mol·L-1的下列各溶液:①盐酸②石
下列事实一定能证明HNO2是弱电解质的是( )①常温下NaNO2溶液的pH大于7②用HNO2溶液做
下列事实一定能证明HNO2是弱电解质的是( )①常温下NaNO2溶液的pH大于7②用HNO2溶液做导电实验,灯泡很暗③HNO2和NaCl不能发生反应④常温下0.1 mol·
(12分)Ⅰ下列物质属于强电解质的是 (填序
(12分)Ⅰ下列物质属于强电解质的是(填序号)①BaCO3②浓硫酸③Al(OH)3④(NH4)2CO3⑤CH3COOH⑥C6H6⑦SO3⑧CsOH⑨H2S⑩Fe(OH)3Ⅱ(1)在粗制CuSO4·5H
能说明醋酸是弱电解质的事实是A.醋酸溶液的导电性比盐酸弱B.醋酸溶液与碳酸钙反应 缓慢放出二氧化碳C
能说明醋酸是弱电解质的事实是A.醋酸溶液的导电性比盐酸弱B.醋酸溶液与碳酸钙反应,缓慢放出二氧化碳C.0 1mol L-1的CH3COOH溶液中氢离子浓度约为0 00
常温下 物质的量浓度为0.01 mol·L-1的醋酸溶液和盐酸 下列说法正确的是A.溶液的pH相同B
常温下,物质的量浓度为0 01 mol·L-1的醋酸溶液和盐酸,下列说法正确的是A.溶液的pH相同B.分别加入足量锌片,盐酸生成的H2体积大C.分别稀释100倍后


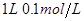 醋酸
醋酸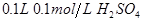 溶液
溶液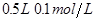 盐酸
盐酸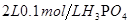 溶液
溶液









