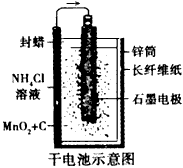
普通锌锰干电池的简图(如图所示) 它是用锌皮制成的锌筒作电极兼作容器 中央插一根碳棒 碳棒顶端加一铜
| 普通锌锰干电池的简图(如图所示),它是用锌皮制成的锌筒作电极兼作容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:Zn+2NH4+ +2MnO2=[Zn(NH3)2]2++Mn2O3+H2O。关于锌锰干电池的下列说法中正确的是 |
 |
| [ ] |
| A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 B.电池正极的电极反应式为:2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O C.电池工作时,电子由正极通过外电路流向负极 D.外电路中每通过0.1mol电子,锌的质量理论上减小6.5 g |
参考解答
| B |
相似问题
下列各变化中 属于原电池反应原理的是[ ]A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.在空
下列各变化中,属于原电池反应原理的是[ ]A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.在空气中金属铝表面迅速氧化成保护层C.红热的铁丝与水接触表面
(1)用锌片 铜片和稀盐酸组成的原电池 正极的电极反应式为__________________ 负极
(1)用锌片、铜片和稀盐酸组成的原电池,正极的电极反应式为__________________,负极的电极反应式为__________________,原电池的总反应是____________
某原电池的电池反应为Fe+2Fe3+→3Fe2+ 与此电池反应相符的原电池是[ ]A.铜片
某原电池的电池反应为Fe+2Fe3+→3Fe2+,与此电池反应相符的原电池是[ ]A.铜片、铁片、FeCl3溶液组成的原电池 B.石墨、铁片、Fe(NO3)3溶液组成的原电
过渡排放CO2会造成“温室效应” 科学家正在研究如何将CO2转化为可利用的资源。其中一种方案就是将C
过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为请
构成原电池的化学反应必须具备的特点是 [ ]A.氧化还原反应 B.复分解反应 C.反应的焓变
构成原电池的化学反应必须具备的特点是 [ ]A.氧化还原反应 B.复分解反应 C.反应的焓变小于零D.反应的焓变大于零












