(1)用锌片 铜片和稀盐酸组成的原电池 正极的电极反应式为__________________ 负极
| (1)用锌片、铜片和稀盐酸组成的原电池,正极的电极反应式为__________________,负极的电极反应式为__________________,原电池的总反应是__________________;当有6.5g锌溶解时,则在标准状况下,放出的氢气的体积为________,转移的电子数为__________摩尔,溶液的酸性________(填“增强”或“减弱”)。 (2)选用下列试剂和仪器设计一个原电池。画出装置图。标明原电池的正极、负极、电解质溶液,并写出正极、负极的电极反应。试剂:铜片、铁片、银片、镁条、硫酸铜溶液、硝酸银溶液。仪器:烧杯、导线、铁夹(若还需其它仪器可自己补充) __________________________ |
参考解答
| (1)正极:2H++2e-=H2↑;负极:Zn-2e-=Zn2+;总反应:Zn+2H+=Zn2++H2↑;2.24L;0.2;减弱 |
(2)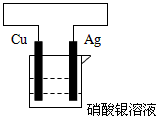 正极为Ag,负极为Cu,电解质溶液为硝酸银溶液 负极:Cu -2e-= Cu2+ 正极:2Ag++2e-=2Ag (答案合理即可) |
相似问题
某原电池的电池反应为Fe+2Fe3+→3Fe2+ 与此电池反应相符的原电池是[ ]A.铜片
某原电池的电池反应为Fe+2Fe3+→3Fe2+,与此电池反应相符的原电池是[ ]A.铜片、铁片、FeCl3溶液组成的原电池 B.石墨、铁片、Fe(NO3)3溶液组成的原电
过渡排放CO2会造成“温室效应” 科学家正在研究如何将CO2转化为可利用的资源。其中一种方案就是将C
过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为请
构成原电池的化学反应必须具备的特点是 [ ]A.氧化还原反应 B.复分解反应 C.反应的焓变
构成原电池的化学反应必须具备的特点是 [ ]A.氧化还原反应 B.复分解反应 C.反应的焓变小于零D.反应的焓变大于零
用铜片 银片 Cu( NO3)2溶液 AgNO3溶液 导线和盐桥(装有琼脂- KNO3的U型管)构成
用铜片、银片、Cu( NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂- KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是 [ ]①在外电路中,
据报道 一种新的电池可能取代目前广泛使用的铅酸蓄电池 它具有容量大的优点。其电池反应为:2Zn+O2
据报道,一种新的电池可能取代目前广泛使用的铅酸蓄电池,它具有容量大的优点。其电池反应为:2Zn+O2=2ZnO,原料为锌、电解液和空气,则下列叙述正确的












