煤化工常常需要研究不同温度F的平衡常数 投料比及热值等问题。已知反应CO(g)+H2O(g)H2(g
| 煤化工常常需要研究不同温度F的平衡常数、投料比及热值等问题。已知反应 CO(g)+H2O(g) 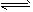 H2(g)+CO2(g)的平衡常数随温度的变化如下表 H2(g)+CO2(g)的平衡常数随温度的变化如下表 |
 |
| 试回答下列问题: (1)上述正向反应的△H____0(填“>”或“<”)。 (2)若在800℃时进行上述反应,各物质以不同的物质的量(单位:mol)组合分别投入恒容反应器,则向正反应方向移动的有_______(填字母编号)。 |
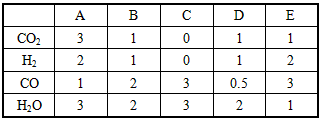 |
| (3)若在500℃时进行上述反应,CO和H2O的起始浓度均为0.020 mol/L,则在该条件下,CO的最大转化率为________。 (4)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5. 60,c(H2CO3)=1.5×10-5 mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3 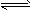 HCO3-+H+的平衡常数K1=___________。 HCO3-+H+的平衡常数K1=___________。(已知:10-5.60= 2.5×10-6) |
参考解答
| (1)< (2)BCE (3)75% (4)4.2×10-7 |
相似问题
把HI气体充入密闭容器中在一定条件下发生反应:2HI(g)H2(g)+I2(g) 在反应趋向化学反应
把HI气体充入密闭容器中在一定条件下发生反应:2HI(g)H2(g)+I2(g),在反应趋向化学反应限度的过程中,下列说法正确的是 [ ]A.HI的生成速率
反应 H2(g)+I2(g)?2HI(g)的平衡常数K1;反应HI(g)?12H2(g)+12I2
反应H2(g)+I2(g)?2HI(g)的平衡常数K1;反应HI(g)?12H2(g)+12I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )A
在体积恒定的密闭容器中 充入3 mo l A和1 mol B发生反应:3A(g)+B(g)xC(g)
在体积恒定的密闭容器中,充入3molA和1molB发生反应:3A(g)+B(g)xC(g),达到平衡后,C在平衡混合气体中的体积分数为φ。若维持温度不变,按1 2molA、0 4
放热反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0在温度t1时达到平衡 c1(CO)
放热反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0在温度t1时达到平衡,c1(CO)=c1(H2O)=1 0mol L,其平衡常数为K1.升高反应体系的温度至t2时,反应
有两个密闭容器A和B A容器内有一个移动的活塞能使容器内保持恒压 B容器能保持恒容。起始时向这两个容
有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等量的体积比为2:1的SO2和O2的混合气












