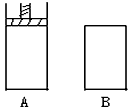
有两个密闭容器A和B A容器内有一个移动的活塞能使容器内保持恒压 B容器能保持恒容。起始时向这两个容
有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B的容积相等。在保持400℃的条件下使之发生如下反应:2SO2+O2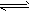 2SO3。 2SO3。 |
|
| (1)达到平衡时所需的时间A容器比B容器________(多、少),A容器中SO2的转化率比B容器中__________ (大、小)。 (2)达到(1)所述平衡后,若向两容器中通入数量不多的等量的He, A容器中化学平衡_________移动(向左、向右、不移动)。 B容器中化学平衡__________移动(向左、向右、不移动)。 (3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数____________;B容器中SO3的物质的量分数____________。(填增大、减小、不变) |
参考解答
| (1)少 ;大 (2)向左 ;不 (3)不变;增大 |
相似问题
已知2SO2 (g)+O2 (g)?2SO3 (g);△H=-197kJ?mol-1.向同温 同体积
已知2SO2(g)+O2(g)?2SO3(g);△H=-197kJ?mol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0 5molO2;
在一个固定体积的密闭容器中 2molA和1molB发生反应2A(g)+ B(g)3C(g)+D(g)
在一个固定体积的密闭容器中,2molA和1molB发生反应2A(g)+ B(g)3C(g)+D(g),达到平衡时,C的浓度为Wmol L。维持容器体积和温度不变,按下列四种配比作为
不同温度下水的电离平衡常数为K(25℃)=1.0×10-14 K(35℃)=2.1×10-14 则下
不同温度下水的电离平衡常数为K(25℃)=1 0×10-14,K(35℃)=2 1×10-14,则下列正确的是( )A.c(H+)随温度的升高而增大B.水的电离过程是放热
将固体NH4I置于密闭容器中 在一定温度下发生下列反应: ①NH4I(s)NH3(g)+HI(g);
将固体NH4I置于密闭容器中,在一定温度下发生下列反应: ①NH4I(s)NH3(g)+HI(g);②2HI(g)H2(g)+I2(g) 达到平衡时,c(H2)=0 5mol L,c(HI)=4mol L
下列叙述中 不正确的是[ ]A.某特定反应的平衡常数不随反应物或生成物的浓度的改变而改变 B
下列叙述中,不正确的是[]A.某特定反应的平衡常数不随反应物或生成物的浓度的改变而改变 B.平衡常数随温度的改变而改变 C.平衡常数发生变化,化学平