(10)(1)氯碱工业是利用电解食盐水生产 ① 为基础的工业体系。(2)电解前 为除去
| (10)(1)氯碱工业是利用电解食盐水生产 ① 为基础的工业体系。 (2)电解前,为除去食盐水中的Mg2+、Ca2+、 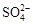 等杂质离子,下列加入顺序合理的是 ②。 等杂质离子,下列加入顺序合理的是 ②。
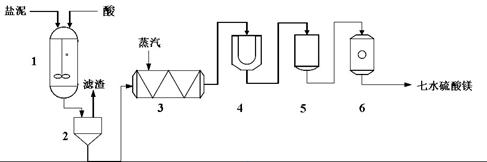 生产七水硫酸镁工艺流程图 1-反应器 2-过滤器 3-蒸发浓缩器 4-结晶槽 5-洗涤槽 6-真空干燥器 装置1中加入的酸应选用 ③ ,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是 ④ 。 装置2中滤渣的主要成分为 ⑤ 。 装置3中通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,此时析出的晶体主要是__⑥__。 用装置6(真空干燥器)干燥七水硫酸镁晶体的理由是 ⑦ 。 |
参考解答
| (1)①氯气、烧碱、氢气(只写出氯气和烧碱也可)。(2分) (2)②D。 (3)③(稀)硫酸。 ④搅拌过程中CO2不断逸出,使平衡CaCO3+H2SO4 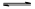 CaSO4+H2CO3(H2O+CO2↑)不断向右移动。(2分) CaSO4+H2CO3(H2O+CO2↑)不断向右移动。(2分)⑤CaSO4、BaSO4、其它不溶物质。(2分) ⑥氯化钠。 ⑦防止失去结晶水。 |
| (1)氯碱工业是利用电解食盐水生产氯气、烧碱、氢气为基础的工业体系。 (2)考查物质的分离和提纯。Ca2+用碳酸钠除去,Mg2+用氢氧化钡除去,SO42-用氯化钡除去,最后加入盐酸酸化。但用于过量的钡离子要用碳酸钠来除,所以碳酸钠必需放在氯化钡和氢氧化钡的后面,因此正确的答案选D。 (3)应用是生成七水硫酸镁,所以应该加入的是稀硫酸;应用在搅拌过程中CO2不断逸出,使平衡CaCO3+H2SO4 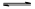 CaSO4+H2CO3(H2O+CO2↑)不断向右移动,所以碳酸钙可以转化为硫酸钙;根据“盐泥”的组成可知,装置2中的不溶物一定含有硫酸钡,同时还含有生成的硫酸钙等其它不溶物质;应用滤液中还含有氯化钠,所以通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,析出的晶体主要是氯化钠;应用在空气中加热硫酸镁晶体易失去结晶水,所以在真空中加热的目的就是防止失去结晶水。 CaSO4+H2CO3(H2O+CO2↑)不断向右移动,所以碳酸钙可以转化为硫酸钙;根据“盐泥”的组成可知,装置2中的不溶物一定含有硫酸钡,同时还含有生成的硫酸钙等其它不溶物质;应用滤液中还含有氯化钠,所以通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,析出的晶体主要是氯化钠;应用在空气中加热硫酸镁晶体易失去结晶水,所以在真空中加热的目的就是防止失去结晶水。 |
相似问题
用阳极甲 阴极乙 电解质溶液丙 在电解过程中补充加入丁物质 可以使电解液的组成保持恒定(物质和浓度与
用阳极甲、阴极乙、电解质溶液丙,在电解过程中补充加入丁物质,可以使电解液的组成保持恒定(物质和浓度与电解前完全相同),下列答案正确的是()甲乙丙
工业上以黄铜矿为原料 采用火法熔炼工艺生产粗钢。(1)该工艺的中间过程会发生反应:2Cu2O+Cu2
工业上以黄铜矿为原料,采用火法熔炼工艺生产粗钢。(1)该工艺的中间过程会发生反应:2Cu2O+Cu2S6Cu+SO2↑,反应的氧化剂是。(2)火法熔炼的粗铜含杂质
(8分)在用惰性电极电解水制取H2和O2时 为了增强导电性 常常要加入一些电解质 下列物质中不能选用
(8分)在用惰性电极电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,下列物质中不能选用的是(填序号)A.NaOH B.H2SO4C.Na2SO4D.C
如图 A池用石墨电极电解NaOH溶液 B池精炼粗铜 一段时间后停止通电 A池中D极产生具有氧化性的气
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2 24L。下列说法正确的是()A.A池溶
(6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液 X和Y是两块电极板。则:(1)若X
(6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液,X和Y是两块电极板。则:(1)若X和Y均为惰性电极,a为饱和的NaCI溶液,则电解时检验Y电












