(6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液 X和Y是两块电极板。则:(1)若X
(6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液,X和Y是两块电极板。则: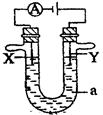 (1)若X和Y均为惰性电极,a为饱和的NaCI溶液,则电解时检验Y电极反应产物的方法是 。 (2)若X、Y分别为石墨和铁,A乃为饱和的NaCl溶液,则电解过程中生成的白色固体物质露置在空气中,可观察到的现象为 。 (3)若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1 mol Cu(OH)2,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。 |
参考解答
| (1)将湿润的淀粉碘化钾试纸靠近Y及支管口,试纸变蓝,说明有氯气生成 (2)白色固体迅速变为灰绿色,最终变为红褐色 (3)0.4 mol |
| (1)Y是阳极产物,所以Y是氯气,极易氯气可以利用其氧化性,即将湿润的淀粉碘化钾试纸靠近Y及支管口,试纸变蓝,说明有氯气生成。 (2)此时铁是阳极,所以铁失去电子,生成亚铁离子。阴极氢离子放电,从而产生氢氧化钠,进而生成氢氧化亚铁沉淀。氢氧化亚铁不稳定,极易被氧气氧化生成氢氧化铁,所以现象就是白色固体迅速变为灰绿色,最终变为红褐色。 (3)向所得溶液中加入0.1 mol Cu(OH)2,恰好恢复电解前的浓度和pH,说明反应中阴极是铜和氢气,阳极生成氧气,根据原子守恒可知,氧气是0.1mol,所以转移电子是0.1mol×4=0.4mol。 |
相似问题
(20分)氯碱工业中电解饱和食盐水的原理示意图 如图所示:(1)溶液A的溶质是
(20分)氯碱工业中电解饱和食盐水的原理示意图,如图所示:(1)溶液A的溶质是;(2)电解饱和食盐水的离子方程式是;(3)电解时用盐酸控制阳极区溶液
(14分)电解原理在化学工业中有广泛应用。下图表示一个电解池 装有电解液a ;X Y是两块电极板 通
(14分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:(1)若X、
用铁作电极 电解500mL 1mol/L CuSO4溶液 当某电极质量增加19.2g时 停止通电。将
用铁作电极,电解500mL 1mol L CuSO4溶液,当某电极质量增加19 2g时,停止通电。将溶液转移至蒸发皿中,蒸干灼烧,得到固体质量为A.77 6 gB.80gC.92 gD.82 7 g
如图所示 将铁棒和石墨棒插入1 L 1 mol?L-1食盐水中。下列说法正确的是A.若电键K与N连接
如图所示,将铁棒和石墨棒插入1 L 1 mol?L-1食盐水中。下列说法正确的是A.若电键K与N连接,铁被保护不会腐蚀B.若电键K与N连接,正极反应式是4OH- -
用铂作电极 电解一定浓度的下列物质的水溶液 电解结束后 向剩余电解液中加适量水 能使溶液和电解前相同
用铂作电极,电解一定浓度的下列物质的水溶液,电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同的是( )A.AgNO3B.H2SO4C.NaOHD.NaCl












