在一定温度下 HCN在水中存在电离平衡:HCNH+ + CN-。下列说法错误的通入HCl气体 Q>K
 在一定温度下,HCN在水中存在电离平衡:HCN 在一定温度下,HCN在水中存在电离平衡:HCN H+ + CN-。下列说法错误的 H+ + CN-。下列说法错误的 通入HCl气体,Q>K,平衡逆向移动 通入HCl气体,Q>K,平衡逆向移动升高温度,溶液pH减小  稀释溶液,电离平衡常数减小 稀释溶液,电离平衡常数减小D.加入NaCN固体, 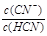 增大 增大 |
参考解答
| C |
答案:C A、正确,通入HCl气体,H+浓度增大,平衡逆向移动; B、正确,电离是吸热反应,升高温度,平衡正向移动,H+浓度增大,溶液pH减小 C、不正确,稀释溶液,电离平衡常数不变; D、正确,CN―浓度增大的幅度大于HCN。 |
相似问题
下列说法不正确的是( )A.Na2CO3溶液中c(OH-)大于c(HCO)B.水的离子积常数为KW
下列说法不正确的是( )A.Na2CO3溶液中c(OH-)大于c(HCO)B.水的离子积常数为KW,若溶液中c2(OH-)=KW,溶液pH可能小于7C.1 mol L的CH3COOH溶液加
描述弱电解质电离情况可以用电离度和电离平衡常数表示 下表是常温下几种弱电解质的电离平衡常数:酸或碱电
描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:酸或碱电离常数(Ka或Kb)CH3COOH1.8×10-5HNO24.6×1
下列说法正确的是A.SO2溶于水 其水溶液能导电 说明SO2是电解质B.测量溶液的导电性可区分出盐酸
下列说法正确的是A.SO2溶于水,其水溶液能导电,说明SO2是电解质B.测量溶液的导电性可区分出盐酸和醋酸,导电能力强的是盐酸C.NaHCO3溶液中有:HCO3—
下列物质中 不能导电的电解质是A.氯酸钾溶液B.澄清石灰水C.酒精D.氯化钠晶体
下列物质中,不能导电的电解质是A.氯酸钾溶液B.澄清石灰水C.酒精D.氯化钠晶体
下列事实或变化 能证明一水合氨是弱电解质的是( )A.氨水受热分解挥发出氨气B.氨水与醋酸反应
下列事实或变化,能证明一水合氨是弱电解质的是()A.氨水受热分解挥发出氨气B.氨水与醋酸反应生成醋酸铵,而醋酸铵是强电解质C.氨水的导电能力弱D.












