在pH=12.00时 用0.01 mol.dm-3EDTA滴定20.00 cm30.01 mol.d
在pH=12.00时,用0.01 mol.dm-3EDTA滴定20.00 cm30.01 mol.dm-3Ca2+溶液,计算下列各情况时的pCa:(a)滴定前;(b)消耗19.98 am3EDTA时;(c)消耗20.00 cm3EDTA时;(d)消耗20.02 cm3EDTA时。
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:(a)在滴定开始前溶液中Ca3+浓度和pCa为 c(Ca2+)=0.01 mol.dm-3pCa=一lg 0.01=2.0; (b)在加入19.98 cm3EDTA溶液后溶液中Ca2+浓度和pCa为 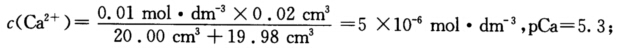 (c)在化学计量点时假定Ca2+与EDTA全部反应形成CaY2-配离子此时
(c)在化学计量点时假定Ca2+与EDTA全部反应形成CaY2-配离子此时  这种情况不可能出现。实际上c(CaY2-)c(Ca2+)c(Y4-)的数值将决定pH=12.00时的条件稳定常数。
这种情况不可能出现。实际上c(CaY2-)c(Ca2+)c(Y4-)的数值将决定pH=12.00时的条件稳定常数。 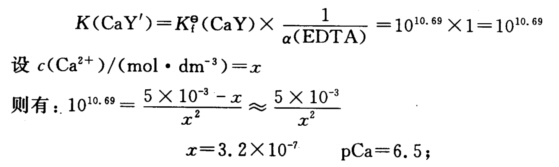 (d)在加入19.98 cm3EDTA溶液后如果忽略由平衡产生的Y4-离子则
(d)在加入19.98 cm3EDTA溶液后如果忽略由平衡产生的Y4-离子则 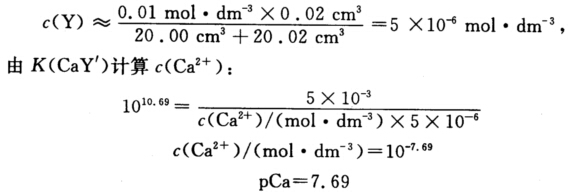
(a)在滴定开始前溶液中Ca3+浓度和pCa为c(Ca2+)=0.01mol.dm-3,pCa=一lg0.01=2.0;(b)在加入19.98cm3EDTA溶液后,溶液中Ca2+浓度和pCa为(c)在化学计量点时假定Ca2+与EDTA全部反应形成CaY2-配离子,此时这种情况不可能出现。实际上,c(CaY2-),c(Ca2+),c(Y4-)的数值将决定pH=12.00时的条件稳定常数。(d)在加入19.98cm3EDTA溶液后,如果忽略由平衡产生的Y4-离子,则
相似问题
已知PbSO4+2e-===Pb+SO42- Eθ=一0.359 V Pb2++2e-===Pb E
已知PbSO4+2e-===Pb+SO42- Eθ=一0.359 V Pb2++2e-===Pb Eθ=一0.126 V Ksp(PbSO4)为 ( )A.3.4×10-6B.4.6×10-7C.1.2×10-8D.1.6×10-9请帮忙给出正确答案和分析,谢谢!
已知Eθ(Cu2+/Cu+)=+0.159 V Eθ(Cu2+/CuI)=+0.869 V 则可以计
已知Eθ(Cu2+/Cu+)=+0.159 V,Eθ(Cu2+/CuI)=+0.869 V,则可以计算出Ksp(CuI)为 ( )A.2.4×10-24B.4.3×10-18C.8.6×10-15D.1.0×10-12请帮忙给出正确答案和分析,谢谢!
CaF2沉淀在pH=4的溶液中的溶解度较pH=6溶液中的溶解度 ( )A.小B.大C.相等D.可能大
CaF2沉淀在pH=4的溶液中的溶解度较pH=6溶液中的溶解度 ( )A.小B.大C.相等D.可能大也可能小请帮忙给出正确答案和分析,谢谢!
KMnO。标准溶液和Na2S2O3标准溶液在配制时都需将水煮沸 请比较两者在操作上的不同 并解释其原
KMnO。标准溶液和Na2S2O3标准溶液在配制时都需将水煮沸,请比较两者在操作上的不同,并解释其原因。请帮忙给出正确答案和分析,谢谢!
一般同离子效应将使沉淀溶解度________________。请帮忙给出正确答案和分析 谢谢!
一般同离子效应将使沉淀溶解度________________。请帮忙给出正确答案和分析,谢谢!












