若A为强酸根 存在可与金属离子形成络合物的试剂L 则难溶化合物MA在水中溶解度的计算式为______
若A为强酸根,存在可与金属离子形成络合物的试剂L,则难溶化合物MA在水中溶解度的计算式为________________。
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案: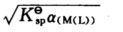
相似问题
已知FeS的Kspθ=6.0×10-18 H2 S的Ka1θ×Ka2θ=9.23×10-22 则在0
已知FeS的Kspθ=6.0×10-18,H2 S的Ka1θ×Ka2θ=9.23×10-22,则在0.10 mol dm-3的Fe2+溶液中通入H2S至饱和,欲使FeS不沉淀,溶液的pH应是 ( )A
已知:Kspθ(Ag2 CrO4)=1.1×10-12 Kspθ(AgCl)=1.8×10-10。则
已知:Kspθ(Ag2 CrO4)=1.1×10-12,Kspθ(AgCl)=1.8×10-10。则反应:Ag2 CrO4(s)+2Cl-====2AgCl(s)+CrO42-的Kθ= ________________。请帮忙给出正确答案和分析,谢谢!
Ag2CrO4在0.001 0 mol.dm2 AgNO3溶液中的溶解度较在0.001 0 mol.
Ag2CrO4在0.001 0 mol dm2 AgNO3溶液中的溶解度较在0.001 0 mol dm2 K2CrO4中的溶解度相等。 ( )此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!
海水中Mg2+浓度大约有0.059 mol.dm-3 在工业提取镁的过程中 首先把Mg2+转化成Mg
海水中Mg2+浓度大约有0.059 mol dm-3,在工业提取镁的过程中,首先把Mg2+转化成Mg(OH)2沉淀,然后再提取。如果一个海水样的OH-浓度为2.0×10-3mol dm-
欲配制pH=5.09的醋酸盐缓冲溶液 需向0.300 dm3 0.25 mol.dm-3的HAc溶液
欲配制pH=5.09的醋酸盐缓冲溶液,需向0.300 dm3 0.25 mol dm-3的HAc溶液中加入多少克NaAc?请帮忙给出正确答案和分析,谢谢!












