硫酸工业中存在如下反应:2SO2(g)+O2(g)2SO3(g) △H
硫酸工业中存在如下反应:2SO2(g)+O2(g)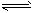 2SO3(g) △H<0 2SO3(g) △H<0 (1)写出该反应的平衡常数表达式_______,升高温度平衡常数_______(填“不变”、“增大”、“减小”)。 (2)该反应达平衡后,若只增大压强,平衡将向_______方向移动;若只升高温度,平衡向_______方向移动。 (3)实际生产中要用过量的空气,原因是______________;还需加入催化剂,目的是______________;不在高温下进行该反应的理由是______________。 |
参考解答
(1)K=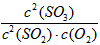 ;减小 ;减小(2)正反应;逆反应 (3)增大来源丰富、成本低的反应物浓度,提高SO3产量;加快反应速率;该反应为放热反应,温度太高尽管反应速率快,但产量低 |
相似问题
乙醇可通过淀粉等生物质原料发酵制得 属于可再生资源 通过乙醇制取氢气具有良好的应用前景。已知通过乙醇
乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气具有良好的应用前景。已知通过乙醇制取氢气有如下两条路线: a.水蒸气催化重整
甲醇被称为21世纪的新型燃料 工业上通过下列反应①和② 用CH4和H2O为原料来制备甲醇。 ①CH4
甲醇被称为21世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。 ①CH4(g)+H2O(g)CO(g)+3H2(g) △H1 ②CO(g)+2H2(g)CH3OH(g)
在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g)pC(g)。 (1)欲使A与B的转化率
在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g)pC(g)。 (1)欲使A与B的转化率等于m:n,则起始加入A、B的物质的量之比为__________;(2)充入一
在密闭容器中有可逆反应:nA(g)+mB(g)pC(g) ΔH>0处于平衡状态(已知n+m>p) 则
在密闭容器中有可逆反应:nA(g)+mB(g)pC(g) ΔH>0处于平衡状态(已知n+m>p),则下列说法正确的是[ ]①升温,c(B) c(C)的比值变小 ②降温时体系内混
某温度下 体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)Z(g)+W(s) △H>0 下列
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)Z(g)+W(s) △H>0 下列叙述正确的是 [ ]A 加入少量W,逆反应速率增大 B 当容器中












