在一个体积固定的密闭容器中 进行的可逆反应A(s)+3B(g)3C (g) 。下列叙述中表明可逆反应
在一个体积固定的密闭容器中,进行的可逆反应A(s)+3B(g)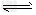 3C (g) 。下列叙述中表明可逆反应一定达到平衡状态的是 3C (g) 。下列叙述中表明可逆反应一定达到平衡状态的是 |
| [ ] |
| ①C的生成速率与C的分解速率相等; ②单位时间内生成amol A,同时生成3amol B; ③B的浓度不再变化; ④混合气体总的物质的量不再发生变化; ⑤A、B、C的物质的量之比为1:3:3; ⑥混合气体的密度不再变化; ⑦B的生成速率与C的生成速率之比为1:1 。 A.①②③⑦ B.①③④⑥⑦ C.①③⑥⑦ D.①③④⑤⑦ |
参考解答
| C |
相似问题
当一个可逆反应进行到正反应速率与逆反应速率相等的时候 就达到了“化学平衡”.对于化学平衡的下列说法中
当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”.对于化学平衡的下列说法中正确的是( )①化学反应达到化学平衡时,
恒温时 将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g)?xC
恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g)?xC(g)+D(s),10s时,测得A的物质的量为1 7mol,C的反应速率为0 022
可逆反应2NO2?2NO+O2在体积固定的密闭容器中达到平衡状态的标志是( )①单位时间内生成n
可逆反应2NO2?2NO+O2在体积固定的密闭容器中达到平衡状态的标志是( )①单位时间内生成nmolO2的同时生成2nmolNO2②单位时间内生成nmolO2的同时生成2n
用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件 能大幅度提高发动机的热效率.工业上用化学气相
用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g
在一定温度下 反应A2(g)+B2(g)?2AB(g)达到平衡的标志是(NA代表阿伏加德罗常数)(
在一定温度下,反应A2(g)+B2(g)?2AB(g)达到平衡的标志是(NA代表阿伏加德罗常数)( )A.单位时间生成NA的A2同时生成NA的ABB.容器内的总压不












