关于下图装置的叙述 错误的是A.铜是正极 其质量不变B.氢离子在铜表面被氧化 产生气泡C.电流从铜片
关于下图装置的叙述,错误的是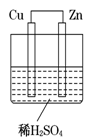
|
参考解答
| B |
答案:B A、正确,锌是负极,质量减少,铜是正极,其质量不变 B、不正确,氢离子得电子,在铜表面被还原,产生气泡 C、正确,电流从铜片经导线流向锌片,与电子流向相反。 D、正确,锌活泼,失电子,电子从锌片经导线流向铜片。 |
相似问题
钢铁发生吸氧腐蚀时 负极上发生的电极反应是( )A.2H+ + 2e- ='==' H2↑B.Fe
钢铁发生吸氧腐蚀时,负极上发生的电极反应是()A.2H+ + 2e- = "== " H2↑B.Fe == Fe2+ + 2e-C.2H2O + O2 + 4e- = "== " 4OH-D.Fe3+ + e- = "== " Fe2+
在由铜锌组成的原电池(电解质是稀硫酸)中 有位同学在铜电极收集到了标准状况下22.4L的气体 (1
在由铜锌组成的原电池(电解质是稀硫酸)中,有位同学在铜电极收集到了标准状况下22 4L的气体, (1) (1分)铜锌原电池的总反应的离子方程式为:______
把a b c d四块金属浸泡在稀H2SO4中 用导线两两相连可组成原电池。若a b相连时 a为负极;
把a、b、c、d四块金属浸泡在稀H2SO4中,用导线两两相连可组成原电池。若a、b相连时,a为负极;c、d相连时,c为负极,a、c相连时,c为正极,b、d相连时,b
下图为甲烷燃料电池原理示意图 按照此图的提示 下列叙述不正确的是( )A.a电极是负极B.b电极
下图为甲烷燃料电池原理示意图,按照此图的提示,下列叙述不正确的是()A.a电极是负极B.b电极的电极反应为:4OH- -4e- →2H2O +O2 ↑ C.甲烷燃
已知:下列说法不正确的是A.该反应原理可用于设计氢氧燃料电池B.破坏1molH-O键需要的能量是46
已知:下列说法不正确的是A.该反应原理可用于设计氢氧燃料电池B.破坏1molH-O键需要的能量是463 4kJC.H2O(g)=H2(g)+1 2O2(g)△H="+241 8" kJ molD.H2












