已知:下列说法不正确的是A.该反应原理可用于设计氢氧燃料电池B.破坏1molH-O键需要的能量是46
已知: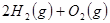 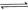 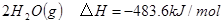 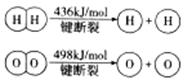 下列说法不正确的是
|
参考解答
| D |
| 原电池中必须有电子的转移,所以只有氧化还原反应才能设计成原电池,A正确。反应热是断键吸收的能量和形成化学键所放出的能量的差值,因此有2×436kJ/mol+498kJ/mol-2×2×akJ/mol=-483.6kJ/mol,解得a=463.4,所以选项B正确。正反应是放热反应,则逆反应就是吸热反应,C正确。化学键越强越牢固,因此根据键能可知,水中H-O比氢气中H-H键牢固,D不正确,答案选D。 |
相似问题
图1是在金属锌板上贴上一张用某溶液浸湿的滤纸 图2是NaBH4/H2O2燃料电池 则下列说法正确的是
图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4 H2O2燃料电池,则下列说法正确的是A.图2电池放电过程中,Na+从正极区向负极区迁移B.图2电
关于下图所示装置的叙述 正确的是( )A.铜是阳极 铜片上有气泡产生B.铜离子在铜片表面被还原C
关于下图所示装置的叙述,正确的是()A.铜是阳极,铜片上有气泡产生B.铜离子在铜片表面被还原C.电流从锌片经导线流向铜片D.正极附近的SO42-离子浓度
(12分)将锌片和铜片用导线相连后一同插入稀硫酸中 导线上便有电流通过。(1)锌片为___ ___
(12分)将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过。(1)锌片为______(填“正极”或“负极”),电极反应是。(2)铜片为_______
如下图所示的锌和铜及稀硫酸组成的原电池中 有下列说法 其中不正确的是:( ) A.铜棒上有气体放
如下图所示的锌和铜及稀硫酸组成的原电池中,有下列说法,其中不正确的是:() A.铜棒上有气体放出,溶液pH变大B.锌是正极,铜是负极C.导线中有电子流
某原电池工作时总的反应为Zn+Cu2+===Zn2++Cu 该原电池的组成可能是 A.Zn为正极
某原电池工作时总的反应为Zn+Cu2+===Zn2++Cu,该原电池的组成可能是A.Zn为正极,Cu为负极,CuCl2溶液作电解质溶液B.Cu为正极,Zn为负极,稀H2SO4作电解












