右图表示反应X(g)4Y(g)+Z(g) ΔH
右图表示反应X(g) 4Y(g)+Z(g),ΔH<0,在某温度时 4Y(g)+Z(g),ΔH<0,在某温度时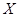 的浓度随时间变化的曲线: 的浓度随时间变化的曲线:下列有关该反应的描述正确的是 
|
参考解答
| B |
| 从图像可以看出,反应进行到6min时X的浓度不再发生变化,说明此时反应达到了平衡状态,A不正确。X在第一分钟和第二分钟内其浓度的变化量分别是0.3mol/L和0.2mol/L,所以其速率之比为3:2,B正确。反应后气体的物质的量是增加的,所以反应的过程是熵增大的过程,C不正确。温度降低,反应速率均减小,D不正确。答案B。 |
相似问题
可逆反应 2A (气) + 3B (气) 2C (气) + D(气) 在四种不同条件下反应速率最快
可逆反应 2A (气) + 3B (气) 2C (气) + D(气),在四种不同条件下反应速率最快的是A.VA = 0 5mol (L·min)B.VB = 0 6mol (L·min)C.VC = 0 35mol (L·min)D.VD = 0 4mol (L·min)
可逆反应2SO2 + O2 2SO3 如果SO2的起始浓度为2 mol/L 2min后SO2的浓
可逆反应2SO2 + O2 2SO3,如果SO2的起始浓度为2 mol L ,2min后SO2的浓度为1 8mol L,则用SO2的浓度变化表示的反应速率为:A.1mol/(L·min)B.0 9
在2A(g)+B(g) 3C(g)+4D(g)中 下列情况能够降低该反应速率的是A.升高温度B.减
在2A(g)+B(g) 3C(g)+4D(g)中,下列情况能够降低该反应速率的是A.升高温度B.减小压强C.使用催化剂D.增大A的浓度
当温度高于40℃时 铜的平均溶解速率随着反应温度升高而下降 其主要原因是
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是。⑷在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀
在反应A(g) + 2B(g) = 2C(g)中 1s内A的物质的量浓度减少0.1mol/L 则用C
在反应A(g) + 2B(g) = 2C(g)中,1s内A的物质的量浓度减少0 1mol L,则用C表示的化学反应速率为()A.0 1mol (L S)B.0 2mol (L S)C.0 01mol (L S)D.0 02mol (L S)


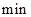 后,反应就终止了
后,反应就终止了









