硫酸铵是一种常用的铵态氮肥.下表是硫酸铵化肥品质的主要指标.指标项目优等品一等品合格品外观白色结晶
硫酸铵是一种常用的铵态氮肥.下表是硫酸铵化肥品质的主要指标.
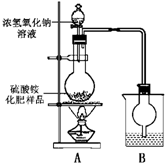 . [观察外观] 该硫酸铵化肥无可见机械杂质. [实验探究] 按如图所示装置进行实验. (1)烧瓶内发生反应的离子方程式为:______烧杯中盛放的试剂最好是______(填“浓硫酸”、“稀硫酸”或“水”) (2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是______ [交流讨论] 甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:______ 乙同学:实验装置中还存在另一个明显缺陷是:______ 经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验 [探究结论] 称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重3.4g.得出探究结论为______. | ||||||||||||
参考解答
(1)硫酸铵和氢氧化钠反应生成硫酸钠、水和氨气,反应方程式为:(NH4)2SO4+2NaOH
故答案为:NH4++OH-
(2)氢氧化钠的浓溶液,电离出的氢氧根离子浓度大,与铵根离子反应的氢氧根离子浓度大,加热温度高,反应速度快,所以,加入足量浓氢氧化钠溶液并充分加热,能使硫酸铵充分反应完全转化为NH3, 故答案为:使硫酸铵充分反应完全转化为NH3; [交流讨论制取氨气为氢氧化钠溶液与硫酸铵固体反应,所以生成的氨气中含有水蒸气,随氨气一同进入B装置中,影响氨气的质量,影响含氮量的测定,所以需增加一个干燥装置;反应装置中各部分都残留氨气,需将反应装置中残留的氨气赶出, 故答案为:A、B装置间缺一个干燥装置;缺少赶尽反应装置中残留氨气的装置; [探究结论 增重的3.4g为氨气的质最,设13.5g样品中含有(NH4)2SO4的质量为x: (NH4)2SO4+2NaOH
132 34 x 3.4g 132:34=x:3.4g 解得:x=13.2g
故答案为:该化肥为合格品; |
相似问题
下列所选用试剂(仪器自选)能达到实验目的是( )A.探究同周期非金属元素性质递变规律:氯水 溴化钾
下列所选用试剂(仪器自选)能达到实验目的是( )A.探究同周期非金属元素性质递变规律:氯水、溴化钾、碘化钾、四氯化碳B.探究+4价硫既有氧化性又
某研究性学习小组将实验室制备二氧化碳气体反应后的废物进行处理 目的是制取中性干燥剂CaCl2.得到固
某研究性学习小组将实验室制备二氧化碳气体反应后的废物进行处理,目的是制取中性干燥剂CaCl2.得到固体后,他们对固体的成分进行了如下探究:[提出猜想]
鉴别下列各组物质的水溶液所选的试剂(括号内)中不正确的是( )A.白酒 食醋(NaHCO3溶液)B
鉴别下列各组物质的水溶液所选的试剂(括号内)中不正确的是( )A.白酒、食醋(NaHCO3溶液)B.葡萄糖、福尔马林[新制Cu(OH)2悬浊液]C.食盐、纯
某100mL溶液中仅含下表中的5种离子(不考虑水的电离及离子的水解) 且各离子的物质的量均为0.1m
某100mL溶液中仅含下表中的5种离子(不考虑水的电离及离子的水解),且各离子的物质的量均为0 1mol.阴离子SO42-、NO3-、Cl-阳离子Fe3+、Fe2+、NH4+、Cu2
探究过氧化氢的性质该化学兴趣小组根据所提供的实验条件设计了两个实验 分别证明了过氧化氢的氧化性和不稳
探究过氧化氢的性质该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯












