将0.6 mol A和0.5 mol B充入0.4L密闭容器中发生2A(g)+B(g)mD(g)+E
将0.6 mol A和0.5 mol B充入0.4L密闭容器中发生2A(g)+B(g)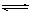 mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是( ) mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是( )A.A、B均转化了20% B.m值为1 C.5min内用A表示的平均反应速率为0.1 mol·L-1·min-1 D.平衡时混合物总物质的量为1 mol |
参考解答
| B |
| 考查可逆反应的有关计算。根据E的反应速率可知,生成E的物质的量是0.1 mol·L-1·min-1×0.4L×5min=0.2mol,所以计量数m=1。则 2A(g)+B(g) 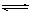 D(g)+E(g) D(g)+E(g)起始量(mol) 0.6 0.5 0 0 转化量(mol) 0.4 0.2 0.2 0.2 平衡量(mol) 0.2 0.3 0.2 0.2 所以A和B的转化率分别为 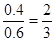 、 、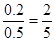 ,因此选项A不正确。 ,因此选项A不正确。因为速率之比是相应的化学计量数之比 所以5min内用A表示的平均反应速率为0.1 mol·L-1·min-1×2=0.2 mol·L-1·min-1 平衡时混合物总物质的量为0.2mol+0.3mol+0.2mol+0.2mol=0.9mol 所以答案选B。 |
相似问题
(10分)为了研究碳酸钙与盐酸反应的反应速率 某同学通过下图实验装置测定反应中生成的CO2气体体积
(10分)为了研究碳酸钙与盐酸反应的反应速率,某同学通过下图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线,在该实验过程中发现锥形瓶
已知:4NH(g)+5O(g)4NO(g)+6HO(g) 若反应速率分别用v(NH) v(O) v(
已知:4NH(g)+5O(g)4NO(g)+6HO(g),若反应速率分别用v(NH)、v(O)、v(NO)、V(HO)[mol (L·min)]表示,则下列关系正确的是A.4v(NH)=5
(8分)在25℃时 向100 mL含氯化氢14.6 g的盐酸溶液里放入5.6 g纯铁粉(不考虑反应前
(8分)在25℃时,向100 mL含氯化氢14 6 g的盐酸溶液里放入5 6 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末收集到氢气1 12 L(标
甲 乙两个容器内都在进行A→B的反应 甲中每分钟减少4 mol A 乙中每分钟减少2 mol A 则
甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减少2 mol A,则两容器中的反应速率A.甲快B.乙快C.相等D.无法确定
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)2C(气),若经 2 s(秒)后测得 C












