已知Ksp[Al(OH)3]=1.3×10-33 mol4·L-4 Ksp[Fe(OH)3]=4.
已知Ksp[Al(OH)3]=1.3×10-33 mol4·L-4, Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4。现向pH=0浓度均为0.04mol·L-1的Al3+、Fe3+溶液中加入NaOH溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是( )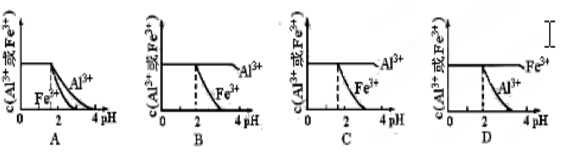 |
参考解答
| B |
试题分析:依据已知的Ksp[Al(OH)3=1.3×10-33 mol4·L-4、Ksp[Fe(OH)3=4.0×10-38 mol4·L-4,可以求得Cu2+和Fe3+完全以氢氧化物沉淀时(即金属离子浓度小于10-5mol·L-1时)的pH分别为:4.7和3.2;现在向pH=0浓度均为0.04mol?L-1的Al3+、Fe3+溶液中,调节PH值,(设溶液体积不变),所以氢氧化钠溶液提高溶液PH到3.2,氢氧根离子浓度增大,使Qc大于Ksp,三价铁离子能沉淀完全,根据Ksp[Fe(OH)3=4.0×10-38,=[Fe3+[OH-3,计算得[OH-=10-12mol/L;三价铁离子开始生成沉淀的PH=2,所以铁离子开始沉淀到沉淀完全的PH范围为2-3.2过程中该过程中Al3+、Fe3+的浓度与pH关系依据图象和反应原理判断,当PH=2时,铁离子开始沉淀,故B选项正确。 |
相似问题
(14分) CuCl是有机合成的重要催化剂 并用于颜料 防腐等工业。工业上由废铜料(含Fe Al及其
(14分) CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:物质开始沉
下列说法中正确的是( )A.难溶电解质在水溶液中达到沉淀溶解平衡时 沉淀和溶解即停止B.Ksp越小
下列说法中正确的是( )A.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止B.Ksp越小,难溶电解质在水中的溶解能力一定越弱C.Ksp的大小与离
下表是五种银盐的溶度积常数Ksp(25℃) 下列说法不正确的是化学式AgClAg2SO4Ag2SAg
下表是五种银盐的溶度积常数Ksp(25℃),下列说法不正确的是化学式AgClAg2SO4Ag2SAgBrAgI溶度积1 4×10-101 4×10-56 3×10-507 7×10-138 51×10-16A.2
已知如下物质的溶度积常数:FeS:Ksp=6.3×10-18mol2·L-2;CuS:Ksp=1.3
已知如下物质的溶度积常数:FeS:Ksp=6 3×10-18mol2·L-2;CuS:Ksp=1 3×10-36mol2·L-2。 下列说法正确的是A.同温度下,CuS的溶解度大于FeS的溶解度B.
现有等浓度的下列溶液:(1)NaHSO4 (2)NH4Cl (3)CH3COONa (4)NaCl
现有等浓度的下列溶液:(1)NaHSO4 (2)NH4Cl (3)CH3COONa (4)NaCl (5)NaOH (6)Ba(OH)2 (7)H2SO4 按溶液pH由小到大排列 [ ]A.(1)(2)(4)(5)(3)(7)












