25℃时 下列溶液中微粒的物质的量浓度关系正确的是 [ ]A.pH=7的NaHSO3与Na
| 25℃时,下列溶液中微粒的物质的量浓度关系正确的是 |
|
[ ] |
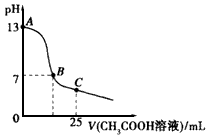
| A.pH=7的NaHSO3与Na2SO3混合溶液中:3c(Na+) =c(HSO3-)+c(SO32-) B.0.1 mol·L-1的KHA溶液,其pH=10:c(K+)>c(HA-)>c( OH-)> c(H+) C.20 mL 0.1 mol·L-1醋酸钠溶液与10 mL 0.1 mol·L-1盐酸混合后的溶液中:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) D.在25 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1 CH3COOH溶液,溶液pH变化如上图所示,在A、B间任一点,溶液中一定都存在下列关系: c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
参考解答
| BC |
相似问题
某酸式盐NaHY的水溶液呈碱性 下列叙述正确的是[ ]A.H2Y的电离方程式:H2Y+2H2
某酸式盐NaHY的水溶液呈碱性,下列叙述正确的是[ ]A.H2Y的电离方程式:H2Y+2H2OY2-+2H3O+B.离子的水解方程式:HY-+H2OH2Y+OH-C.该酸式盐溶液中离子浓
将0.2mol/LCH3COONa与0.1mol/LHCl等体积混合 混合后溶液的pH小于7。(假设
将0 2mol LCH3COONa与0 1mol LHCl等体积混合,混合后溶液的pH小于7。(假设体积变化忽略不计)则溶液中下列微粒的物质的量浓度关系正确的是:[ ]A.c(CH3
对下列各溶液中 微粒的物质的量浓度关系表述正确的是 [ ]A.0.1mol·L-1的(NH
对下列各溶液中,微粒的物质的量浓度关系表述正确的是 [ ]A.0 1mol·L-1的(NH4)2SO4溶液中:c(SO42- )>c(NH4+)>c(H+)>c(OH-) B.0 1 mol·L-1的NaH
25℃时 有关弱酸的电离常数如下表 下列说法正确的是 [ ]A.相等物质的量浓度的溶液的pH
25℃时,有关弱酸的电离常数如下表,下列说法正确的是 [ ]A.相等物质的量浓度的溶液的pH关系:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) B.相等物质的量浓
下表为元素周期表的一部分 请参照元素①~⑧在表中的位置 回答下列问题(1)写出由④ ⑤ ⑧元素中形成
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题(1)写出由④、⑤、⑧元素中形成的既含离子键又含共价键的一种离子化合物的电子式