下表为元素周期表的一部分 请参照元素①~⑧在表中的位置 回答下列问题(1)写出由④ ⑤ ⑧元素中形成
| 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题 |
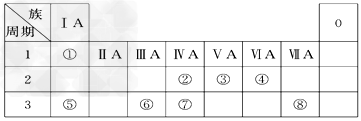 |
| (1)写出由④、⑤、⑧元素中形成的既含离子键又含共价键的一种离子化合物的电子式________。 (2)含元素⑧的单质能与自来水中有机物反应生成对人体有危害的物质,现已逐步淘汰。下列可代替它作自来水消毒剂的是_______ A. NH2Cl B. AlCl3 C. K2FeO4 D. ClO2 (3) W与④是相邻的同主族元素。在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式。 |
 |
| (4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: |
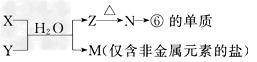 |
| 写出X溶液与Y溶液反应的离子方程式______________, M中阳离子的鉴定方法 __________,如果M中含有元素⑧,M溶液中离子浓度由大到小的排列顺序是______________。 |
参考解答
(1)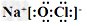 (2)ACD |
(3)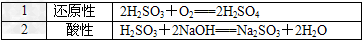 |
| (4)Al3++3NH3·H2O === Al(OH)3+3NH4+;取样,加入NaOH溶液,加热,产生使湿润红色石蕊试纸变蓝的刺激性气体;c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
相似问题
(1)t℃时水的离子积为1×10 -13 则该温度(填“大于” “小于”或“等于”)____ 25℃
(1)t℃时水的离子积为1×10 -13,则该温度(填“大于”、“小于”或“等于”)____ 25℃,其理由是____。若将此温度下pH=11的苛性钠溶液aL 与pH=1的稀
常温下 下列各溶液中微粒的物质的量浓度关系正确的是 [ ]A.0.1mol·L-1的
常温下,下列各溶液中微粒的物质的量浓度关系正确的是 [ ]A 0 1mol·L-1的Na2CO3溶液中:c(Na+)=c(CO32- )+c(HCO3-)+c(H2CO3) B pH=11的Na2CO3溶液中
下列说法正确的是[ ]A. 用甘氨酸()和丙氨酸()缩合最多可形成4种二肽 B. 0.1 m
下列说法正确的是[ ]A 用甘氨酸()和丙氨酸()缩合最多可形成4种二肽 B 0 1mol LNa2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) C 标准状况下,2
某化学研究性学习小组对电解质溶液作如下的归纳总结:(均在常温下) ①常温下 pH=1的强酸溶液 加水
某化学研究性学习小组对电解质溶液作如下的归纳总结:(均在常温下) ①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度一定降低 ②pH=2的盐酸和p
在自然界中 碳及其化合物之间进行着永不停息的转化 这些转化是非常重要的。 (1)在空气中久置的石灰水
在自然界中,碳及其化合物之间进行着永不停息的转化,这些转化是非常重要的。 (1)在空气中久置的石灰水往往会失效,不能再用来检验二氧化碳气体。石灰水












