室温下 将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中 溶液pH和
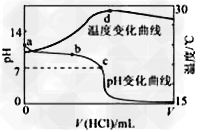
| 室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是 |
 |
| [ ] |
| A. a点由水电离出的c(H+)=1.0×10-14mol/L B. b点:c(NH4+)+c(NH3·H2O)=c(Cl-) C. c点:c(Cl-)= c(NH4+) D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
参考解答
| C |
相似问题
下列推断或表述正确的是 [ ]A.醋酸溶液的pH =a 将此溶液稀释1倍后 溶液的pH =b
下列推断或表述正确的是 [ ]A.醋酸溶液的pH =a,将此溶液稀释1倍后,溶液的pH =b,则a>b B.向2 0 mL浓度均为0 1 moI·L-1的KCl、KI混合液中滴加
A B C D E F六种短周期主族元素 它们的原子序数依次增大。已知:B元素原子的最外层电子数是内
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大。已知:B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其
下列有关电解质溶液中微粒的物质的量浓度关系正确的是[ ]A. 在0.1 mol/L NaHC
下列有关电解质溶液中微粒的物质的量浓度关系正确的是[ ]A 在0 1 mol L NaHCO3溶液中:c(Na+)> c()> c()> c(H2CO3) B 在0 1 mol L Na2CO3溶
室温下 下列有关电解质溶液微粒关系的比较一定正确的是[ ]A.氨水和氯化铵的混合液 当pH=
室温下,下列有关电解质溶液微粒关系的比较一定正确的是[ ]A.氨水和氯化铵的混合液,当pH=7时,c(Cl-) >c(NH4+) B.pH=2的一元酸和pH=12的NaOH溶液等
25℃时 下列溶液中微粒的物质的量浓度关系正确的是 [ ]A.pH=7的NaHSO3与Na
25℃时,下列溶液中微粒的物质的量浓度关系正确的是 [ ]A.pH=7的NaHSO3与Na2SO3混合溶液中:3c(Na+) =c(HSO3-)+c(SO32-) B.0 1 mol·L-1的KHA溶液












