化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的
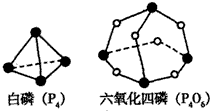
| 化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198KJ·mol-1、 P-O 360kJ·mol-1、氧气分子内氧原子间的键能为498kJ·mol-1则P4+3O2==P4O6的反应热△H为 |
 |
| [ ] |
| A.+1638 kJ·mol-1 B.-1638 kJ·mol-1 C.-126 kJ·mol-1 D.+126 kJ·mol-1 |
参考解答
| B |
相似问题
将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧 生成固态三氧化二硼和液态水 放出649.
将0 3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649 5kJ热量,该反应的热化学方程式为_____________。又已知:H2O
已知1g氢气完全燃烧生成水蒸气时放出热量121 kJ 且氧气中1molO=O键完全断裂时吸收热量49
已知1g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1molO=O键完全断裂时吸收热量496 kJ,水蒸气中1 molH-O键形成时放出热量463 kJ,则氢气中1
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中 破坏1 mol 氢气中的化学键消耗的能量为Q1 kJ
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2 kJ,形
已知破坏1 mol H-H键 Cl-Cl键 H-Cl键分别需要吸收436 kJ 243 kJ 432
已知破坏1 mol H-H键,Cl-Cl键,H-Cl键分别需要吸收436 kJ,243 kJ,432 kJ的能量,则由H2与Cl2生成1 mol HCl的总过程需要[ ]A.放热185 kJ B.吸热185 kJC.放热92 5 kJD.吸热92 5 kJ
白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P
白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ·mol-1、P-O b kJ·mol-1、P===O c kJ·mol-1












