已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g)现在容积均为1L
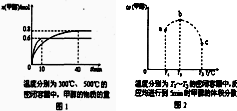
已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g)现在容积均为1L的a、b、c三个密闭容器中分别充入1mol C0和2mol H2的混合气体,控制温度,进行反应,测得相关数据的关系如图1和图2所示.下列说法中不正确的是( )
 |
参考解答
| A、从图1可以看出,甲醇的物质的量为0.6mol的曲线大,说明反应温度高,升高温度,甲醇的物质的量减少,说明正反应是放热反应,故A正确; B、从图2可以看出,反应进行到5min时,a容器的反应如达到平衡,升高温度,平衡向逆向移动,甲醇的体积分数应减小,但图象中给出的是增大,说明还没有达到平衡状态,故B正确; C、达到平衡时,a、b、c三个容器的反应温度不同,a容器温度最低,c容器的反应温度最高,根据反应放热可判断出,升高温度,平衡逆向移动,甲醇的体积分数减小,故应为a>b>c,故C错误; D、b中的平衡状态转变成c中的平衡状态,甲醇的体积分数减小,说明平衡逆向移动,因为反应是放热反应,升高温度,平衡向逆向移动;又知反应物的化学计量数之和大于生成物的,增大压强,平衡逆向移动,故D正确; 故选C. |
相似问题
已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g) 现在容积均为l
已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g) 现在容积均为l L的a、b、c三个密闭容器中分别充入l molCO和2mol H2的混合气体,控制
化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用 如果设法提高化学反应的限度 下面的说法
化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提高化学反应的限度,下面的说法错误的是[ ]A.能够节约原料和能源B.能够提
放热反应CO(g)+H2O(g)?CO2(g)+H2(g)在温度t1时达到平衡 c1(CO)=c1(
放热反应CO(g)+H2O(g)?CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1 0mol L,其平衡常数为K1.升高反应体系的温度至t2时,反应物的平
甲酸甲酯水解反应方程式为:某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的
甲酸甲酯水解反应方程式为:某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表甲酸甲酯转化率在温度T1下随反应
如图所示 某刚性容器内有一活塞和弹簧 B为真空 A内已充入2molSO2和1molO2 在一定条件下
如图所示,某刚性容器内有一活塞和弹簧,B为真空,A内已充入2molSO2和1molO2,在一定条件下发生可逆反应2SO2+O2?2SO3;△H=-QkJ mol,(Q>0)一段时间后












