(4分)工业上用MnO2为原料制取KMnO4 主要生产过程分为两步进行:第一步将MnO2和KOH 粉
| (4分)工业上用MnO2为原料制取KMnO4,主要生产过程分为两步进行:第一步将MnO2和KOH、粉碎,混匀,在空气中加热至熔化,并连续搅拌,制取K2MnO4;第二步将K2MnO4的浓溶液用惰性电极进行电解,在阳极上得到KMnO4,在阴极上得到KOH。电解K2MnO4的浓溶液时,两极发生的电极反应式: 阴极是 ,阳极是 ; 电解的总反应方程式是 。 |
参考解答
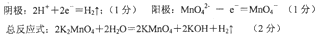 |
由题意在阳极上得到KMnO4,在阴极上得到KOH,阴极是水的电离平衡被破坏,阴极:2H2O +2e―=H2+2OH― ;阳极:MnO42――e―=MnO42― 总反应:2K2MnO4+2H2O=2KMnO4+2KOH+H2↑ |
相似问题
能判断某酸一定是弱电解质的是 ( )A.该酸易挥发B.该酸的稀溶液中有一种分子存在C.导电能力
能判断某酸一定是弱电解质的是 ( )A.该酸易挥发B.该酸的稀溶液中有一种分子存在C.导电能力比盐酸弱D.0 1mol L的该酸溶液中c(H+)为0 001mol L
室温下 将1.00mol ? L-1盐酸滴人20. OO mL 1.OOmol ? L-1的氨水中
室温下,将1 00mol ? L-1盐酸滴人20 OO mL1 OOmol ? L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如下图所示。下列有关说法中不正确的是
在体积都为1L pH都等于2的盐酸和醋酸溶液中 投入0.65g锌粒 则下列各图所示内容比较符合客观事
在体积都为1L、pH都等于2的盐酸和醋酸溶液中,投入0 65g锌粒,则下列各图所示内容比较符合客观事实的是
下列物质中属于强电解质的是A.NH3·H2OB.H2OC.CH3COOHD.醋酸铵
下列物质中属于强电解质的是A.NH3·H2OB.H2OC.CH3COOHD.醋酸铵
水的电离过程为H2OH++OH- 在25℃时水的离子积为:KW=1.0×10-14 在35℃时水的离
水的电离过程为H2OH++OH-,在25℃时水的离子积为:KW=1 0×10-14,在35℃时水的离子积为:KW=2 1×10-14,则下列叙述正确的是 ( )A.水的电离












