水的电离过程为H2OH++OH- 在25℃时水的离子积为:KW=1.0×10-14 在35℃时水的离
水的电离过程为H2O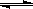 H++OH-,在25℃时水的离子积为:KW=1.0×10-14,在35℃时水的离子积为:KW=2.1×10-14,则下列叙述正确的是 ( ) H++OH-,在25℃时水的离子积为:KW=1.0×10-14,在35℃时水的离子积为:KW=2.1×10-14,则下列叙述正确的是 ( )
|
参考解答
| A |
| 略 |
相似问题
向CH3COOH CH3COO-+ H+ 的平衡体系中 加入下列物质能使醋酸的电离程度和溶液的pH
向CH3COOHCH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是()A.NH4Cl固体B.CH3COONaC.NH3·H2OD.Zn粉
一定温度下 往纯水中加入少量下列物质。当物质溶于水(或与水反应)后 水的电离可能不受影响的是A.盐B
一定温度下,往纯水中加入少量下列物质。当物质溶于水(或与水反应)后,水的电离可能不受影响的是A.盐B.酸C.碱D.氧化物
PH=3的盐酸和醋酸各100mL 分别和锌反应 反应完后 放出的气体一样多。若最后有一溶液中锌剩余
PH=3的盐酸和醋酸各100mL,分别和锌反应,反应完后,放出的气体一样多。若最后有一溶液中锌剩余,则下列判断正确的是 ( )A.反应开始时速率v(HCl)>
写出下列物质在水溶液中的电离方程式:NH3·H2O:
写出下列物质在水溶液中的电离方程式:NH3·H2O:, Ba(OH)2:___________________________,NaHSO4:, NaHCO3:___________________________ 。
常温下 0.1mol/L氨水中c(H+)/c(OH-)=1×10-10 下列说法正确的是A.溶液中由
常温下,0 1mol L氨水中c(H+) c(OH-)=1×10-10,下列说法正确的是A.溶液中由水电离出的c(OH-)=1×10-10mol LB.溶液中c(OH-)+c(NH3·H2O)=0 1m












