已知25℃时 电离常数Ka(HF)=3.6×10-4 mol·L-1 溶度积常数KSP(CaF2)=
| 已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3。现向1L 0.2 mol·L-1HF溶液中加入1L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是 |
| [ ] |
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 B.该体系中有CaF2沉淀产生 C.该体系中KSP(CaF2)= 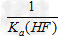 D.KSP(CaF2)随温度和浓度的变化而变化 |
参考解答
| B |
相似问题
已知铅蓄电池放电过程可以表示为PbO2 + 2 H2SO4 + Pb='2' PbSO4 + 2H2
已知铅蓄电池放电过程可以表示为PbO2 + 2 H2SO4 + Pb="2" PbSO4 + 2H2O下列关于铅蓄电池的说法正确的是A.Pb为正极,PbO2为负极B.正极电极反应
人造地球卫星用的一种高能电池——银锌电池 该电池的电极反应式为:Zn+2OH- -2e- = ZnO
人造地球卫星用的一种高能电池——银锌电池,该电池的电极反应式为:Zn+2OH- -2e- = ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-,据此判断氧化银是()A
如图所示 将铁 铜通过导线相连 置于稀硫酸中.(1)铁片上的现象是______ 电极反应式_____
如图所示,将铁、铜通过导线相连,置于稀硫酸中.(1)铁片上的现象是______,电极反应式______.(2)铜片上的现象是______,电极反应式______.(3)写
随着人们生活质量的不断提高 废电池进行集中处理的问题被提到议事日程 其首要原因是( )。A.利用电
随着人们生活质量的不断提高,废电池进行集中处理的问题被提到议事日程,其首要原因是( )。A.利用电池外壳的金属材料B.防止电池中汞、镉和铅等金属离子
汽车的启动电源常用铅蓄电池。其结构如下图所示 放电时其电池反应如下:PbO2+Pb+2H2SO42P
汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时其电池反应如下:PbO2+Pb+2H2SO42PbSO4+2H2O。下列叙述中正确的是( )A.Pb是正极B.PbO2得












