如图所示 将铁 铜通过导线相连 置于稀硫酸中.(1)铁片上的现象是______ 电极反应式_____
| 如图所示,将铁、铜通过导线相连,置于稀硫酸中. (1)铁片上的现象是______,电极反应式______. (2)铜片上的现象是______,电极反应式______. (3)写出该电池总反应的离子方程式______. (4)Fe2+向______(填具体电极)移动,溶液中的pH______(填“变大”或“变小”). 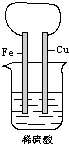 |
参考解答
| (1)该原电池中,铁的活泼性大于铜,铁作负极,铁失电子变成离子进入溶液,所以铁片逐渐溶解,电极反应式为:Fe-2e-=Fe2+; 故答案为:Fe-2e-=Fe2+. (2)铜作正极,铜电极上,氢离子得电子生成氢气2H++2e-=H2↑,所以看到的现象是:有大量气泡产生. 故答案为:有大量气泡产生;2H++2e-=H2↑. (3)正负极上电极反应式相加得电池反应式,所以电池反应式为Fe+2H+=Fe2++H2↑; 故答案为:Fe+2H+=Fe2++H2↑. (4)该电池外电路上,电子从铁片沿导线流向铜片,所以铜片上有大量电子,根据异性电荷相吸,所以 Fe2+向铜极移动,在铜极上氢离子得电子生成氢气,所以氢离子浓度降低,溶液中的pH变大. 故答案为:变大. |
相似问题
随着人们生活质量的不断提高 废电池进行集中处理的问题被提到议事日程 其首要原因是( )。A.利用电
随着人们生活质量的不断提高,废电池进行集中处理的问题被提到议事日程,其首要原因是( )。A.利用电池外壳的金属材料B.防止电池中汞、镉和铅等金属离子
汽车的启动电源常用铅蓄电池。其结构如下图所示 放电时其电池反应如下:PbO2+Pb+2H2SO42P
汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时其电池反应如下:PbO2+Pb+2H2SO42PbSO4+2H2O。下列叙述中正确的是( )A.Pb是正极B.PbO2得
下列关于Cu—Zn原电池的说法正确的是 A.在原电池中 电子流出的一极为负极B.原电池中 发生还原反
下列关于Cu—Zn原电池的说法正确的是 A.在原电池中,电子流出的一极为负极B.原电池中,发生还原反应的电极是负极C.原电池中,电流的方向是从负极到正
在铜锌原电池中 盛有浓度为的稀硫酸200ml 工作一段时间后 在正极收集气体224ml(标准状况下)
在铜锌原电池中,盛有浓度为的稀硫酸200ml,工作一段时间后,在正极收集气体224ml(标准状况下)。(1)负极的反应式是_________________________,正极
如将两个铂电极插入KOH溶液中 向两极分别通入CH4和O2 即构成甲烷燃料电池。已知通入甲烷的一极
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH—-8e-CO32—+7H2O,下列叙述正确的是












