如图所示 甲 乙两池电极材料都是铁棒和碳棒 请回答下列问题:(1)若两池中均为CuSO4溶液 反应一
| 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: (1)若两池中均为CuSO4溶液,反应一段时间后: ①有红色物质析出的是甲池中的______棒,乙池中的______棒. ②乙池中阳极的电极反应式是______. (2)若两池中均为饱和NaCl溶液: ①写出乙池中总反应的离子方程式______. ②甲池中碳极上电极反应式是______,乙池碳极上电极反应属于______(填“氧化反应”或“还原反应”). ③若乙池转移0.02mol e-后停止实验,池中溶液体积是200mL,则溶液混合均匀后的所得NaOH溶液的物质的量浓度为______. 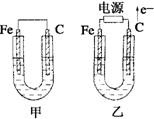 |
参考解答
| (1)①甲池为原电池,原电池中活泼金属做负极,发生氧化反应,碳棒做正极,有Cu析出,乙池为电解池,外电路电子流向电源正极,所以碳棒为阳极,放出氯气,阴极铁电极上发生还原反应有Cu析出,故答案为:碳;铁; ②乙池中,惰性电极为阳极,电解硫酸铜溶液,阳极氢氧根离子放电生成氧气,电极反应为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑; (2)①若电解质溶液为饱和氯化钠溶液,则乙池就是用惰性电极为阳极电解氯化钠溶液,方程式为:2NaCl+2H2O
故答案为:2NaCl+2H2O
②甲池中碳棒为正极,发生还原反应,氧气得到电子生成氢氧根,与吸氧腐蚀的电极反应相同,O2+2H2O+4e-=4OH-,乙装置中,碳棒是阳极,发生失电子的氧化反应, 故答案为:O2+2H2O+4e-=4OH-;氧化反应; ③电解氯化钠溶液的方程式为:2NaCl+2H2O
|
相似问题
如图所示甲 乙两电化学装置(一个为原电池 一个为电解池) 其电极材料都是铁棒与碳棒 装置部分外电路未
如图所示甲、乙两电化学装置(一个为原电池,一个为电解池),其电极材料都是铁棒与碳棒,装置部分外电路未画完整,若两装置中均盛放CuSO4溶液,一段时间
有两只串联的电解池 甲池盛有CuSO4溶液 乙池盛有一定量某硝酸盐的稀溶液 电解时当甲池电极质量增加
有两只串联的电解池,甲池盛有CuSO4溶液,乙池盛有一定量某硝酸盐的稀溶液,电解时当甲池电极质量增加1 6 g Cu时,乙池析出5 4 g固体,则乙池的溶质可
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:将6 mol CO2和8 mol H2充入2
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中
如图为铜铁原电池示意图 下列有关说法正确的是( )A.铜棒逐渐溶解B.该装置能将电能转化为化学能C
如图为铜铁原电池示意图,下列有关说法正确的是( )A.铜棒逐渐溶解B.该装置能将电能转化为化学能C.电子由铁棒通过导线流向铜棒D.正极反应为Fe-2e-=Fe2+
有如图装置:回答下列问题:(1)装置A是______池 B是______池.(2)装置A中的Zn极是
有如图装置:回答下列问题:(1)装置A是______池,B是______池.(2)装置A中的Zn极是______极,Cu极上的电极反应方程式为:______.(3)装置B中是浓度












