如图所示甲 乙两电化学装置(一个为原电池 一个为电解池) 其电极材料都是铁棒与碳棒 装置部分外电路未
| 如图所示甲、乙两电化学装置(一个为原电池,一个为电解池),其电极材料都是铁棒与碳棒,装置部分外电路未画完整,若两装置中均盛放CuSO4溶液,一段时间后甲池中的碳棒和乙池中的铁棒均有红色物质析出.请回答下列问题: (1)甲是______(填写装置名称,下同);乙是______. (2)甲乙装置中铁电极的名称分别是______、______. (3)甲乙装置中碳电极上发生反应的电极反应式分别是.甲:______;乙:______. (4)若两装置中均盛放饱和NaCl溶液.则甲池中碳电极的电极反应式为______.现乙装置中转移0.02mol电子后停止实验,装置中溶液的体积是200mL,则此时溶液中c(OH-)=______(不考虑产物的相互反应). 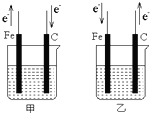 |
参考解答
| (1)甲装置中电子从铁电极出来,乙装置中电子向铁电极移动,由此说明能自发的进行氧化还原反应是甲,乙不能自发的进行氧化还原反应,所以甲是原电池,乙是电解池, 故答案为:原电池,电解池; (2)甲池中铁易失电子而作负极,乙池中铁上得电子发生氧化反应,所以铁作阴极, 故答案为:负极,阴极; (3)甲池中碳棒作正极,正极上铜得电子发生还原反应,电极反应式为:2Cu2++2e-=Cu,乙池中碳棒作阳极,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑, 故答案为:甲:2Cu2++2e-=Cu,乙:4OH--4e-=2H2O+O2↑; (4)①如果甲池中是氯化钠溶液,则铁发生吸氧腐蚀,正极上氧气得电子发生还原反应,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-; ②乙池中电解氯化钠溶液时,阳极上氯离子放电,阴极上氢离子放电,所以电池反应式为:2NaCl+2H2O
故答案为:0.1mol?L-1. |
相似问题
有两只串联的电解池 甲池盛有CuSO4溶液 乙池盛有一定量某硝酸盐的稀溶液 电解时当甲池电极质量增加
有两只串联的电解池,甲池盛有CuSO4溶液,乙池盛有一定量某硝酸盐的稀溶液,电解时当甲池电极质量增加1 6 g Cu时,乙池析出5 4 g固体,则乙池的溶质可
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:将6 mol CO2和8 mol H2充入2
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中
如图为铜铁原电池示意图 下列有关说法正确的是( )A.铜棒逐渐溶解B.该装置能将电能转化为化学能C
如图为铜铁原电池示意图,下列有关说法正确的是( )A.铜棒逐渐溶解B.该装置能将电能转化为化学能C.电子由铁棒通过导线流向铜棒D.正极反应为Fe-2e-=Fe2+
有如图装置:回答下列问题:(1)装置A是______池 B是______池.(2)装置A中的Zn极是
有如图装置:回答下列问题:(1)装置A是______池,B是______池.(2)装置A中的Zn极是______极,Cu极上的电极反应方程式为:______.(3)装置B中是浓度
某学生欲完成2HCl+Cu═CuCl2+H2↑反应 设计了如图所示的四个实验 可行的实验是( )A
某学生欲完成2HCl+Cu═CuCl2+H2↑反应,设计了如图所示的四个实验,可行的实验是( )A.B.C.D.












