(11 分)科学家一直致力研究常温 常压下“人工固氮”的新方法。曾有实验报道:在常温 常压 光照条件
(11 分)科学家一直致力研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3,反应的化学方程式如下:N2(g)+ 3H2O(l) 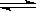 2NH3(g)+ O2(g)。回答下列问题: 2NH3(g)+ O2(g)。回答下列问题:(1)进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105 Pa、反应时间3 h),则该反应的正反应为 反应(填“吸热”或“放热”)
(3)合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部分物质的燃烧热数 据如下: H2(g) :△H =-285.8 kJ?mol-1; CO(g) :△H =-283.0 kJ?mol-1; CH4(g) :△H =-890.3 kJ?mol-1。 已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式__________________________________。 (4)有人设想寻求适合的催化剂和电极材料,以N2、H2为电极反应物,以HCl——NH4Cl为电解质溶液制成新型燃料电池,请写出该电极的正极反应式 (5)生成的NH3可用于制铵态氮肥,如(NH4)2SO4、NH4Cl,这些肥料显 性,原因是(用离子方程式表示)___________________________,使用时避免与________________物质合施。 |
参考解答
| ( 11 分) (1)吸热 (2)升高温度. 增大N2的浓度 (3)CH4(g)+H2O(g)=CO(g)+3H2(g) △ H=+206.1 kJ?mol-1 (4) N2+8H+ + 6e— =' 2' NH4+ (5)酸性 NH4++H2O 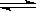 NH3 H2O+H+ 碱性 NH3 H2O+H+ 碱性 |
| 略 |
相似问题
工业上电解食盐水的阴极区产物是()A.氯气B.氢气和氯气C.氢气和氢氧化钠D.氯气和氢氧化钠
工业上电解食盐水的阴极区产物是()A.氯气B.氢气和氯气C.氢气和氢氧化钠D.氯气和氢氧化钠
如图是一套电化学装置 对其有关说法错误的是( )A.装置A是原电池 装置B是电解池B.反应一段时间
如图是一套电化学装置,对其有关说法错误的是( )A.装置A是原电池,装置B是电解池B.反应一段时间后,装置B中溶液PH增大C.a口若消耗1molCH4,d口可
由铜 锌和稀硫酸组成的原电池工作时 电解质溶液的酸性( )A.不变B.逐渐减弱C.逐渐增强D.先减
由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的酸性( )A.不变B.逐渐减弱C.逐渐增强D.先减弱,后增强
与下列图像有关的说法正确的是A根据图①可判断A2(g)+3B2(g)2AB3(g)的ΔH>0B.图②
与下列图像有关的说法正确的是A根据图①可判断A2(g)+3B2(g)2AB3(g)的ΔH>0B.图②表示压强对2A(g)+B(g)3C(g)的影响,甲的压强大C.图③表示乙酸溶液中通
如图所示 某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理 其中乙装置
如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.根据要求回答相关问题:(1)通入













