对于反应A(g)+3B(g)2C(g) 下列各数据表示不同条件下的反应速率 其中反应进行得最快的是A
对于反应A(g)+3B(g) 2C(g),下列各数据表示不同条件下的反应速率, 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是 A.v(A)=0.2mol/(L?s) B.v(B)="0.2" mol/(L?s) C.v(B)=0.3mol/(L?s) D.v(C)=0.2mol/(L?s) |
参考解答
| A |
试题分析:化学反应速率之比等于化学计量系数之比,因此可得: 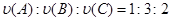 。 。A、v(A)=0.2mol/(L?s) 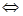 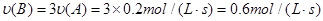 D、v(C)=0.2mol/(L?s) 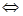 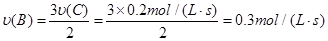 因此,反应速率最大的为A。 点评:本题考查了反应速率的计算,属于基础题。掌握反应速率的计算公式即可。 |
相似问题
(8分)在2L密闭容器内 800℃时反应:2NO(g)+O2(g)2NO2(g)体系中 n(NO)随
(8分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:时间(s)012345n(NO)(mol)0 0200 0100 0080 0070 0070 007(
甲 乙两容器内都在进行A→B的反应 甲中每分钟减少4 mol 乙中每分钟减少2 mol 则两容器中的
甲、乙两容器内都在进行A→B的反应,甲中每分钟减少4 mol,乙中每分钟减少2 mol,则两容器中的反应速率A.甲快B.乙快C.相等D.无法判断[
在N2+3H22NH3的反应中 在5s中N2由6mol/L减至2mol/L。则NH3的平均反应速率是
在N2+3H22NH3的反应中,在5s中N2由6mol L减至2mol L。则NH3的平均反应速率是 ( )A.0 08 mol (L·s)B.0 8 mol (L·s)C.1 6mol (L·s)D.2 4 mol (L·s)
反应A+3B=2C+2D在四种不同情况下的反应速率分别为:①v(A)=0.15mol/(L·s)②v
反应A+3B=2C+2D在四种不同情况下的反应速率分别为:①v(A)=0.15mol/(L·s)②v(B)=0.6mol/(L·s)③v(C)=0.4 mol/(L·s)④v(D)=0.45 mol/(L·s)
把0.6 mol 气体X 和0.4 mol 气体Y混合于2.0L的密闭容器中 发生如下反应3X(g)
把0 6 mol 气体X 和0 4 mol 气体Y混合于2 0L的密闭容器中,发生如下反应3X(g)+ Y(g)nZ(g)+2W(g),测得5min末已生成0 2 mol W,又知以Z表












