(10分)(1)高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe Ni Ag A
| (10分) (1)高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe、Ni、Ag、Au等四种金属杂质,可用电解法进行精炼制得高纯铜。 请在如图中标明电极材料和电解质溶液的名称 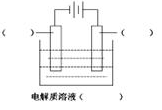 已知Ni的金属活动性介于Fe和Sn之间。则精炼完成后,在阳极底部的沉积物中可回收到的金属为 ________(填化学式)。 (2)若在实验室中完成此实验,可用铅蓄电池做电源。铅蓄电池的电池总反应式为: 2PbSO4+2H2O  Pb+PbO2+4H++2SO42- Pb+PbO2+4H++2SO42-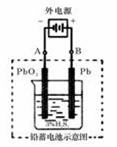 在完全放电耗尽PbO2和Pb时,若按上图所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”) (3)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色稀溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重0.16 g。请回答下列问题: 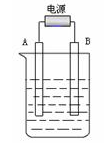 ①B电极的反应式_____________________。 ②原溶液的物质的量浓度是_________________;电解后溶液的pH为 ________。(假设电解前后溶液的体积不变) |
参考解答
| (1)左 精铜 右 粗铜 硫酸铜溶液 Ag、Au (2)Pb PbO2 B (3)①4OH――4e-=2H2O+O2↑ ②0.005mol/L 2 |
| 考查电化学原理的应用 (1)粗铜精炼时,粗铜和电源的正价相连,作阳极。纯铜和电源的负极相连,作阴极,电解质溶液是硫酸铜溶液。纯铜中含有的杂质铁和镍的活泼性均强于铜的,所以二者首先失去电子。银和金的活泼性弱于铜的,在铜存在的条件下,二者不可能失去电子,二者最终形成阳极泥。 (2)根据装置图可判断A和电源的负极相连,作阴极,得到电子发生还原反应,电极反应式 为PbSO4+2e-=Pb+SO42-。B和电源的正极相连,作阳极,失去电子发生氧化反应,电极反应式为PbSO4-2e-+ 2H2O = PbO2 + 4H+ +SO42-。所以A极生成铅,B极生成二氧化铅,因此蓄电池的正负极的极性将对换,即B将是正极。 (3)根据溶液显蓝色,以及析出红色的固态物质可判断,该固态物质一定是铜,铜;离子在阴极达到电子,析出铜单质,电极反应式为Cu2++2e-=Cu。则B极是阳极,且生成的气体是无色的,所以是溶液中OH―放电,失去电子,发生氧化反应生成氧气,电极反应式为4OH――4e-=2H2O+O2↑。电极增重0.16 g,即铜是0.16g,物质的量为 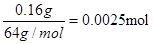 ,所以原溶液的浓度为 ,所以原溶液的浓度为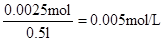 。每消耗1mol铜离子,则同时生成2mol氢离子,所以氢离子的浓度为0.005mol/L×2=0.11mol/L,因此pH=2。 。每消耗1mol铜离子,则同时生成2mol氢离子,所以氢离子的浓度为0.005mol/L×2=0.11mol/L,因此pH=2。 |
相似问题
利用电解法可将含有Fe Zn Ag Pt等杂质的粗铜提纯 下列叙述正确的是A.电解时以纯铜作阳极B.
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是A.电解时以纯铜作阳极B.电解时阴极发生氧化反应C.粗铜连接电源负极,其电极反应
下列关于电解的说法正确的是A.电解是把化学能转变成电能B.电解池的阳极发生氧化反应 阴极发生还原反应
下列关于电解的说法正确的是A.电解是把化学能转变成电能B.电解池的阳极发生氧化反应,阴极发生还原反应C.电解时溶液中靠电子导电D.工业上通过电解熔
四个电解装置都以Pt做电极 它们分别装着如下电解质溶液进行电解 电解一段时间后 测定其pH变化 所记
四个电解装置都以Pt做电极,它们分别装着如下电解质溶液进行电解,电解一段时间后,测定其pH变化,所记录的结果正确的是ABCD电解质溶液HClAgNO3BaCl2KOHp
用惰性电极电解500 mL CuSO4溶液 电解一段时间后 发现阴极增重0.064 g(假设电解时该
用惰性电极电解500 mL CuSO4溶液,电解一段时间后,发现阴极增重0 064 g(假设电解时该电极无H2析出,且不考虑水解和溶液体积变化),此时溶液中c(H+)
以黄铜矿精矿为原料 制取硫酸铜及金属铜的工艺如下所示:Ⅰ.将黄铜矿精矿(主要成分为CuFeS2 含有
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:Ⅰ 将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎Ⅱ 采用如下装置进行电化学












