以黄铜矿精矿为原料 制取硫酸铜及金属铜的工艺如下所示:Ⅰ.将黄铜矿精矿(主要成分为CuFeS2 含有
| 以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示: Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎 Ⅱ.采用如下装置进行电化学浸出实验 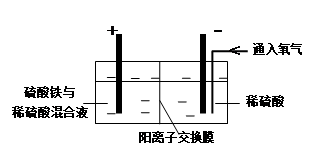 将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂。 Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应: 2RH(有机相)+ Cu2+(水相)  R2Cu(有机相)+ 2H+(水相) R2Cu(有机相)+ 2H+(水相)分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。 Ⅳ.电解硫酸铜溶液制得金属铜。 (1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应: CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S↓+ 2H+ ① 阳极区硫酸铁的主要作用是 。 ② 电解过程中,阳极区Fe3+的浓度基本保持不变,原因是 。 (2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。写出上述现象对应的反应式 。 (3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是 ;加入有机萃取剂的目的是 。 (4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是 。 (5)步骤Ⅳ,若电解200mL0.5 mol/L的CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是 。 |
参考解答
| (16分) (1)①吸收硫化氢气体,防止环境污染(1分) ②Fe2+- e-→Fe3+(1分) (2)2H++2 e-→H2↑ Cu2++2e-→Cu 2Cu+O2+2H2SO4=2CuSO4+2H2O(各1分) (3)分液漏斗 (1分) 富集Cu2+,分离Cu2+与其它金属阳离子 (2分,每个要点1分) (4)增大H+浓度,使平衡2RH(有机相) + Cu2+(水相)  R2Cu(有机相)+ 2H+(水相)逆向移动,Cu2+进入水相得以再生(1分) R2Cu(有机相)+ 2H+(水相)逆向移动,Cu2+进入水相得以再生(1分)(5) c(H+)>c(SO42-)>c(Cu2+)>c(OH-)(2分) |
试题分析: (1)根据反应:CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S↓+ 2H+①可知硫酸铁作用为吸收硫化氢气体,防止环境污染;②吸收硫化氢气体要消耗Fe3+ ,而其浓度不变必须Fe2+在阳极放电:Fe2+- e-→Fe3+。 (2)根据题中现象和离子放电规律可知:2H++2 e-→H2↑ Cu2++2e-→Cu 2Cu+O2+2H2SO4=2CuSO4+2H2O(各1分) (3)分离互不相容的液体要使用分液漏斗 ; 萃取的作用在于富集Cu2+,分离Cu2+与其它金属阳离子。 (4)根据题意可知:增大H+浓度,使平衡2RH(有机相) + Cu2+(水相)  R2Cu(有机相)+ 2H+(水相)逆向移动,Cu2+进入水相得以再生。 R2Cu(有机相)+ 2H+(水相)逆向移动,Cu2+进入水相得以再生。(5)电解200mL0.5 mol/L的CuSO4溶液,生成铜3.2 g时,相当于等浓度的CuSO4和硫酸的混合液,其中Cu2+部分水解,得c(H+)>c(SO2- 4)>c(Cu2+)>c(OH-)。 |
相似问题
H2O中加入等物质的量的Ag+ Na+ Ba2+ NO3- SO42- Cl- 该溶液放在惰性电极的
H2O中加入等物质的量的Ag+、Na+、Ba2+、NO3-、SO42-、Cl-,该溶液放在惰性电极的电解槽中通电片刻后,氧化产物与还原产物的质量比是 ( )A.1∶8B.8∶1
在100 mLCuSO4的溶液中 用石墨作电极电解一段时间 两极均收到2.24L气体(标准状况) 则
在100 mLCuSO4的溶液中,用石墨作电极电解一段时间,两极均收到2 24L气体(标准状况),则原溶液中,Cu2+的物质的量浓度为 ()A.1mol?L―1B.2mol?L
用惰性电极电解CuSO4溶液一段时间后 欲使溶液恰好恢复至电解前情况 可加入的物质是 (
用惰性电极电解CuSO4溶液一段时间后,欲使溶液恰好恢复至电解前情况,可加入的物质是 ( )A.CuSO4B.Cu(OH)2C.CuD.CuO
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液 理论上两极所得气体的体积随时间变化的关系
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信
用铂电极(惰性)电解下列溶液时 阴极和阳极上的主要产物分别是H2和O2的是( )A.NaCl溶液B.
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是()A.NaCl溶液B.HCl溶液C.稀NaOH溶液D.酸性AgNO3溶液












