已知反应AsO43- +2I- +2H+AsO33-+ I2+H2O是可逆反应。设计如图装置(C1
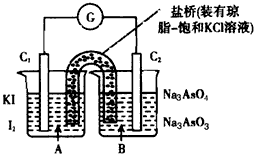
已知反应AsO43- +2I- +2H+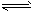 AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作: AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:Ⅰ.向B烧杯中逐滴加入浓盐酸 Ⅱ.向B烧杯中逐滴加入40%NaOH溶液结果发现电流计指针均发生偏转据此,下列判断正确的是 |
 |
| [ ] |
| A. 操作Ⅰ过程中,C1为正极 B. 操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 C. Ⅰ操作过程中,C2棒上发生的反应为AsO43-+2H++2e-→AsO33-+H2O D. Ⅱ操作过程中,C1棒上发生的反应为2I-→I2+2e- |
参考解答
| C |
相似问题
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片 下列叙述正确的是[ ]A.正极附近的S
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是[ ]A.正极附近的SO42-浓度逐渐增大 B.电子通过导线由铜片流向锌片 C.正极有O2
下列关于铜锌原电池(装置如下图)的说法 正确的是[ ]A.是电能转化为化学能的装置 B.Zn
下列关于铜锌原电池(装置如下图)的说法,正确的是[ ]A.是电能转化为化学能的装置 B.Zn片作正极 C.Cu片上有气泡产生D.电流计指针不发生偏转
在A B C三个烧杯中分别盛有相同体积 相同物质的量浓度的NaNO3 HCl和KCl溶液 用石墨作电
在A、B、C三个烧杯中分别盛有相同体积、相同物质的量浓度的NaNO3、HCl和KCl溶液,用石墨作电极将它们串联起来进行电解,一段时间后,电解液pH增大的烧杯
(1)某同学用碳棒 铜棒和稀硫酸为原材料 实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=
(1)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。请在下边画出能够实验这一反应的装置图。__
下图为某原电池的结构示意图 下列说法中不正确的是[ ]A.原电池工作时的总反应为Zn+Cu2
下图为某原电池的结构示意图,下列说法中不正确的是[ ]A.原电池工作时的总反应为Zn+Cu2+==Zn2++Cu该反应一定为放热反应B.原电池工作时,Zn电极流出电












