(1)某同学用碳棒 铜棒和稀硫酸为原材料 实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=
| (1)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应: Cu+H2SO4(稀)=CuSO4+H2↑。请在下边画出能够实验这一反应的装置图。_____________________ (2)某同学在做一定条件下铜与稀硫酸的反应实验时,看到碳棒上有气泡产生,但铜棒却没有被腐蚀。请你分析其原因:_________________________。 |
参考解答
(1)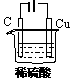 (2)两极与电源的正负极接反了,或铜棒接电源的负极了。 |
相似问题
下图为某原电池的结构示意图 下列说法中不正确的是[ ]A.原电池工作时的总反应为Zn+Cu2
下图为某原电池的结构示意图,下列说法中不正确的是[ ]A.原电池工作时的总反应为Zn+Cu2+==Zn2++Cu该反应一定为放热反应B.原电池工作时,Zn电极流出电
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液 其充 放
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2OCd(OH)2+2Ni(OH)2。有关
(1)火力发电是通过化石燃料燃烧 产生的热量使水气化为蒸汽 推动蒸汽轮机 然后带动发电机发电。从能量
(1)火力发电是通过化石燃料燃烧,产生的热量使水气化为蒸汽,推动蒸汽轮机,然后带动发电机发电。从能量转换角度看,火力发电的系列能量转换过程是:__
下列关于铜-锌-稀硫酸构成的原电池的有关叙述 错误的是[ ]A.锌做负极 锌发生氧化反应B.
下列关于铜-锌-稀硫酸构成的原电池的有关叙述,错误的是[ ]A.锌做负极,锌发生氧化反应B.铜做正极,铜不易失去电子而受到保护C.负极发生还原反应,正
下列表述中 合理的是 [ ]A. 把SO2通入品红试液 可验证SO2水溶液的酸性 B. 构成
下列表述中,合理的是 [ ]A 把SO2通入品红试液,可验证SO2水溶液的酸性 B 构成如图所示装置时,盐桥中的K+移向ZnSO4溶液C 配制一定物质的量浓度












