甲 乙两池电极材料都是铁棒与碳棒 请回答下列问题:(1)若两池中均为CuSO4溶液 反应一段时间后:
| 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题: (1)若两池中均为CuSO4溶液,反应一段时间后: ①有红色物质析出的是甲池中的______棒,乙池中的______棒. ②乙池中阳极的电极反应式是______. (2)若两池中均为饱和NaCl溶液: ①写出乙池中总反应的离子方程式______. ②甲池中碳极上电极反应式是______,乙池碳极上电极反应属于______(填“氧化反应”或“还原反应”). ③将湿润的淀粉KI试纸放在乙池碳极附近,发现试纸变蓝,待一段时间后又发现蓝色褪去.这是因为过量的Cl2将生成的I2又氧化.若反应的Cl2和I2物质的量之比为5:1,且生成两种酸,该反应的化学方程式为______. ④若乙池转移0.02mol e-后停止实验,池中溶液体积是200mL,测溶液混匀后的pH=______. 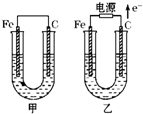 |
参考解答
| 甲装置是原电池,较活泼的金属铁作负极,碳作正极,乙有外接电源属于电解池,根据电子的流向知,碳是阳极,铁是阴极,阳极上失电子发生氧化反应; (1)若两池中均为CuSO4溶液,反应一段时间后,①甲池中,正极上铜离子得电子而析出铜,乙池中,阴极铁棒上铜离子得电子而析出铜; ②乙池中阳极上,氢氧根离子失电子生成氧气和水,电极反应式为:4OH--4e-=2H2O+O2↑, 故答案为:①碳、铁,②4OH--4e-=2H2O+O2↑, (2)若两池中均为饱和NaCl溶液, ①电解氯化钠溶液时,阳极上氯离子失电子生成氯气,阴极上水得电子生成氢气 和氢氧根离子,所以电池反应式为:2Cl-+2H2O
故答案为:2Cl-+2H2O
②甲池中碳极上氧气得电子和水反应生成氢氧根离子,电极反应式为2H2O+O2+4e-=4OH-, 乙池碳极上氯离子失电子发生氧化反应, 故答案为:2H2O+O2+4e-=4OH-,氧化反应; ③过量的Cl2将生成的I2又氧化,氯气被还原生成氯离子,1mol氯气被还原得到2mol电子,若反应的Cl2和I2物质的量之比为5:1,且生成两种酸,根据得失电子数相等知,含碘的酸中碘的化合价是+5价,所以含碘的酸是碘酸,故氯气和碘、水反应生成盐酸和碘酸,反应方程式为:5Cl2+I2+6H2O=2HIO3+10HCl, 故答案为:5Cl2+I2+6H2O=2HIO3+10HCl; ④设生成氢氧化钠的浓度是Cmol/L, 2Cl-+2H2O
2mol 2mol 0.2Cmol 0.02mol C=
答:氢氧化钠溶液的pH=13. |
相似问题
下列说法不正确的是A.纯锌与稀硫酸反应时 为加快速率可滴入少量硫酸铜溶液B.常温下 反应C(s)+C
下列说法不正确的是A.纯锌与稀硫酸反应时,为加快速率可滴入少量硫酸铜溶液B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0C.一定条
(11 分)科学家一直致力研究常温 常压下“人工固氮”的新方法。曾有实验报道:在常温 常压 光照条件
(11 分)科学家一直致力研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水
工业上电解食盐水的阴极区产物是()A.氯气B.氢气和氯气C.氢气和氢氧化钠D.氯气和氢氧化钠
工业上电解食盐水的阴极区产物是()A.氯气B.氢气和氯气C.氢气和氢氧化钠D.氯气和氢氧化钠
如图是一套电化学装置 对其有关说法错误的是( )A.装置A是原电池 装置B是电解池B.反应一段时间
如图是一套电化学装置,对其有关说法错误的是( )A.装置A是原电池,装置B是电解池B.反应一段时间后,装置B中溶液PH增大C.a口若消耗1molCH4,d口可
由铜 锌和稀硫酸组成的原电池工作时 电解质溶液的酸性( )A.不变B.逐渐减弱C.逐渐增强D.先减
由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的酸性( )A.不变B.逐渐减弱C.逐渐增强D.先减弱,后增强












