某温度下 相同pH值的盐酸和醋酸溶液分别加水稀释 平衡pH值随溶液体积变化的曲线如图所示。据图判断正
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积 变化的曲线如图所示。据图判断正确的是( ) 变化的曲线如图所示。据图判断正确的是( ) 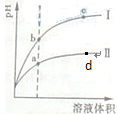 
|
参考解答
| B |
| 醋酸是弱酸,稀释有利于电离,即在稀释过程中,醋酸的酸性要强于盐酸的,所以Ⅱ为醋酸稀释时pH值变化曲线,为盐酸稀释时pH值变化曲线,A、D不正确。B点对应的氢离子浓度大于c点的氢离子,溶液导电性强,B正确。醋酸的电离常数只与温度有关系,C不正确。答案选B。 |
相似问题
向CH3COOH CH3COO-+ H+ 的平衡体系中 加入下列物质能使醋酸的电离程度和溶液的pH
向CH3COOHCH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是A.NH4Cl固体B.CH3COONaC.NH3·H2OD.Zn粉
一定温度下 将一定质量的冰醋酸加水稀释过程中 溶液的导电能力变化如图所示 下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是()A.a、b、c三点溶液的pH: c<a<bB.a、b、c三点醋酸
下列事实不能说明一元酸HA是弱酸的是A.中和一定的NaOH溶液 需消耗与NaOH等物质的量的HAB.
下列事实不能说明一元酸HA是弱酸的是A.中和一定的NaOH溶液,需消耗与NaOH等物质的量的HAB.将pH=4的HA溶液稀释10倍,溶液pH小于5C.将pH=2的HA溶液与pH=
在一定温度下 HCN在水中存在电离平衡:HCNH+ + CN-。下列说法错误的通入HCl气体 Q>K
在一定温度下,HCN在水中存在电离平衡:HCNH+ + CN-。下列说法错误的通入HCl气体,Q>K,平衡逆向移动升高温度,溶液pH减小稀释溶液,电离平衡常数减
下列说法不正确的是( )A.Na2CO3溶液中c(OH-)大于c(HCO)B.水的离子积常数为KW
下列说法不正确的是( )A.Na2CO3溶液中c(OH-)大于c(HCO)B.水的离子积常数为KW,若溶液中c2(OH-)=KW,溶液pH可能小于7C.1 mol L的CH3COOH溶液加












