铁矿石是工业炼铁的主要原料之一 其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素 且杂质不与硫酸反
| 铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与硫酸反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。 Ⅰ.铁矿石中含氧量的测定,以下实验过程不完整,请补充完整。 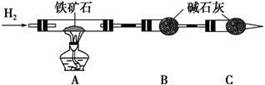 (1)按上图组装仪器,并______________________________________________; (2)将8.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略); (3)从左端导气管口处不断地缓缓通入H2,____________________________, 点燃A处酒精灯; (4)充分反应后,撤掉酒精灯,________________________________________; (5)测得反应后装置B增重2.25 g,则铁矿石中氧的百分含量为________。 Ⅱ.铁矿石中含铁量的测定,流程如下。 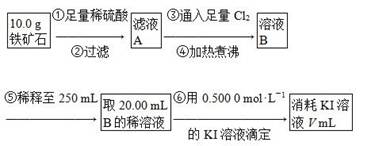 (1)步骤④中煮沸的作用是___________________________________________。 (2)步骤⑤中用到的玻璃仪器有烧杯、胶头滴管、250 mL容量瓶、________。 (3)下列有关步骤⑥的操作中说法正确的是________。 a.因为碘水为黄色,所以滴定过程中不需加指示剂 b.锥形瓶不需要用待测液润洗 c.滴定过程中可利用淀粉溶液作指示剂 d.滴定过程中,眼睛注视滴定管中液面变化 e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数 f.滴定结束后,滴定管尖嘴部分有气泡,则测定结果偏大 (4)若滴定过程中消耗0.500 0 mol·L-1 KI溶液20.00 mL,则铁矿石中铁的百分含量为________。 Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为________。 |
参考解答
| Ⅰ.(1)检查装置的气密性 (3)待装置C出口处氢气验纯后 (4)再持续通入氢气至硬质玻璃管完全冷却 (5)25.0% Ⅱ.(1)赶走溶液中溶解的过量Cl2 (2)玻璃棒 (3)be (4)70.0% Ⅲ.Fe4O5 |
| 本题考查铁矿石中铁的氧化物的化学式的探究。 Ⅰ.实验开始前一定要先检查装置的气密性,再装入药品;在点燃A处酒精灯之前一定要先检验氢气的纯度;撤掉酒精灯后,一定要再通入氢气一段时间,直至硬质玻璃管冷却至室温,以防铁重新被氧化。装置B增加的质量即为生成水的质量,其中m(O)=2.25 g× 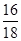 =2.0 g,氧元素的质量分数为 =2.0 g,氧元素的质量分数为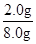 ×100%=25.0%。Ⅱ.(1)因为是用KI溶液进行滴定,但氯气也能与KI反应,影响实验结果,所以必须除去溶液中溶解的氯气。(2)配制一定物质的量浓度的溶液,需要用玻璃棒搅拌、引流。(3)碘水的黄色不明显,a错误。滴定时发生反应:2Fe3++2I-===2Fe2++I2,滴定时如果加入淀粉,则溶液变蓝,但滴定终点时没有颜色变化,所以不能用淀粉作指示剂,c错误。滴定过程中要观察锥形瓶中溶液颜色的变化,不能注视滴定管中液面变化,d错误。滴定结束后,滴定管尖嘴部分有气泡,则所测KI溶液消耗量偏低,测定结果偏低,f错误。 ×100%=25.0%。Ⅱ.(1)因为是用KI溶液进行滴定,但氯气也能与KI反应,影响实验结果,所以必须除去溶液中溶解的氯气。(2)配制一定物质的量浓度的溶液,需要用玻璃棒搅拌、引流。(3)碘水的黄色不明显,a错误。滴定时发生反应:2Fe3++2I-===2Fe2++I2,滴定时如果加入淀粉,则溶液变蓝,但滴定终点时没有颜色变化,所以不能用淀粉作指示剂,c错误。滴定过程中要观察锥形瓶中溶液颜色的变化,不能注视滴定管中液面变化,d错误。滴定结束后,滴定管尖嘴部分有气泡,则所测KI溶液消耗量偏低,测定结果偏低,f错误。(4)根据2Fe3++2I-===2Fe2++I2可知10.0 g铁矿石中,n(Fe)=0.500 0 mol·L-1×0.02 L× 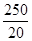 =0.125 mol,m(Fe)=7.0 g,则铁元素的质量分数为70.0%。Ⅲ.铁的氧化物中,n(Fe)∶n(O)= =0.125 mol,m(Fe)=7.0 g,则铁元素的质量分数为70.0%。Ⅲ.铁的氧化物中,n(Fe)∶n(O)=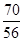 ∶ ∶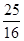 =4∶5,所以其化学式为Fe4O5。 =4∶5,所以其化学式为Fe4O5。 |
相似问题
下列实验可达到实验目的的是:①将与NaOH的醇溶液共热制备CH3—CH═CH2②与适量NaHCO3溶
下列实验可达到实验目的的是:①将与NaOH的醇溶液共热制备CH3—CH═CH2②与适量NaHCO3溶液反应制备③向CH3CH2Br中滴入AgNO3溶液以检验溴元素④用溴水即可
为了比较硫与碳的非金属性的强弱 某同学想通过比较两种元素的最高价氧化物对应的水化物的酸性强弱来证明硫
为了比较硫与碳的非金属性的强弱,某同学想通过比较两种元素的最高价氧化物对应的水化物的酸性强弱来证明硫与碳的非金属性的强弱,采用下图中的甲、乙装
某校学生课外活动小组的同学设计如下图所示实验装置 用来验证一氧化碳具有还原性。回答下列问题(1)装置
某校学生课外活动小组的同学设计如下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题(1)装置B中最适宜的试剂是_______________,其作用是__
在高温时硫铁矿(主要成分FeS2)和氧气反应生成三氧化二铁和二氧化硫(假设硫铁矿中的杂质不参与化学反
在高温时硫铁矿(主要成分FeS2)和氧气反应生成三氧化二铁和二氧化硫(假设硫铁矿中的杂质不参与化学反应)。某化学研究学习小组对硫铁矿样品进行如下实
(10分)某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH 可简写为H2C2
(10分)某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强












