(13分)图4-38中电极a b分别为Ag电极和Pt电极 电极c d都是石墨电极。通电一段时间后 在
(13分)图4-38中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL(标准状态)气体。回答: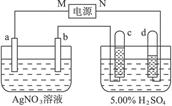 图4-38 (1)直流电源中,M__________为极。 (2)Pt电极上生成的物质是________,其质量为________g。 (3)电源输出的电子,其物质的量与b、c、d各电极分别生成的物质的物质的量之比为:_________∶________∶________∶________。 (4)AgNO3溶液的浓度_______,AgNO3溶液的pH________,H2SO4溶液的浓度______,H2SO4溶液的pH______(填增大、减小或不变)。 (5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为________g。 |
参考解答
| (1)正 (2)Ag 2.16 g (3)4 4 1 2 (4)不变 不变 增大 减小 (5)0.45 |
| (1)用惰性电极电解H2SO4相当于电解水,观察图中c、d两电极上的小试管,根据气体产生的比例,可推断d电极生成的是H2,而c电极生成的是O2,故M为电源的正极,N为电源的负极。 (2)由反应2H2O 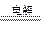 2H2↑+O2↑可知n(H2)∶n(O2)=2∶1,所以该电路中通过的电子物质的量为336 mL/22400 mL·mol-1×2/3×2='0.02' mol。b为Pt电极,也是电解池的阴极,0.02 mol Ag+得0.02 mol电子生成0.02 mol Ag,质量为2.16 g。 2H2↑+O2↑可知n(H2)∶n(O2)=2∶1,所以该电路中通过的电子物质的量为336 mL/22400 mL·mol-1×2/3×2='0.02' mol。b为Pt电极,也是电解池的阴极,0.02 mol Ag+得0.02 mol电子生成0.02 mol Ag,质量为2.16 g。(3)电源输出的电子为0.02 mol,b电极生成的Ag为0.02 mol,c电极生成的O2为0.005 mol,d电极生成的H2为0.01 mol,故四者的比值为4∶4∶1∶2。 (4)a电极作阳极,Ag不断溶解进入溶液,能保持AgNO3溶液相对稳定性,所以AgNO3溶液的浓度不变,pH也不变;而由于H2SO4溶液不断被电解,水量减少,使浓度增大,pH减小。 (5)设原有5.00%的H2SO4溶液的质量为x。则: x×5.00%=(x-336 mL/22400mL·mol-1×2/3×18 g·mol-1)×5.02% 解得:x='0.45' g。 |
相似问题
Ⅰ.用导线将A B两装置的四个电极进行连接 使a极析出铜.回答有关问题.(1)导线将容器A和B连接时
Ⅰ.用导线将A、B两装置的四个电极进行连接,使a极析出铜.回答有关问题.(1)导线将容器A和B连接时,Zn接______,Cu接______(填“a”或“b”)(2)容
如图是三个原电池的装置图.(1)在甲装置中 作为负极的物质是______ 在正极上发生的变化可表示为
如图是三个原电池的装置图.(1)在甲装置中,作为负极的物质是______,在正极上发生的变化可表示为:2H++2e-═H2↑;如果在正极转移了0 2mole-,则在正
由A B C D四种金属按表中装置进行实验 下列叙述中正确的是( )实验装置与现象装置甲乙丙现象二
由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是( )实验装置与现象装置甲乙丙现象二价金属A不断溶解C的质量增加A上有气体产生A.装置
铁棒与石墨棒用导线连接后浸入0.01mol?L-1的食盐溶液中 可能出现的现象是( )A.铁棒附近
铁棒与石墨棒用导线连接后浸入0 01mol?L-1的食盐溶液中,可能出现的现象是( )A.铁棒附近产生OH-B.铁棒逐渐被腐蚀C.石墨棒上放出Cl2D.石墨棒上放出O2
在一密闭容器中 发生反应:A(g)+B(g) C(g)+D(g) 其化学平衡常数K随温度变化的关系如
在一密闭容器中,发生反应:A(g)+B(g) C(g)+D(g),其化学平衡常数K随温度变化的关系如下表所示,则下列有关判断正确的是T ℃8008501 0001 2












